Aproxima-se o período de festas de fim de ano, e com ele as polêmicas uvas-passas. Com elas funciona assim: ou se ama ou se odeia. Mas aqui trago uma outra perspectiva para essa discussão: do ponto de vista de segurança de alimentos, elas são mesmo seguras?
O principal vilão: micotoxinas
A presença de micotoxinas, e mais especificamente da ocratoxina A, é a principal razão para remessas de uvas-passas serem impedidas de acessar o mercado europeu. Isso porque o processo de secagem de uvas para obtenção das passas, na maior parte das vezes, ocorre por exposição ao sol. Tais condições favorecem o desenvolvimento de fungos produtores de toxina, principalmente a ocratoxina A (OTA). Diversas notificações do sistema RASFF (Rapid Alert System for Food and Feed) da União Europeia demonstram a sua alta ocorrência, além de evidências de recolhimento pelo MAPA (Ministério da Agricultura, Pecuária e Abastecimento) no Brasil, em 2023 e em 2022, quando uvas-passas que seriam utilizadas para produção de panetones foram apreendidas.
Perigos microbiológicos
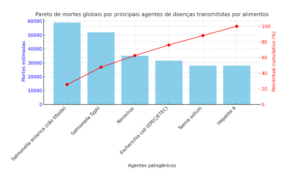
Apesar da baixa atividade de água após o processo de secagem, alguns microrganismos se mantêm viáveis até obter condições favoráveis para proliferação. Entre eles, nos preocupam os famosos patógenos Salmonella, E. coli e Listeria monocytogenes. Como exemplo, entre 2008 e 2009, mais de cinquenta pessoas foram reportadas com salmonelose, das quais 21 tiveram que ser hospitalizadas, todas relacionadas ao consumo de frutas secas.
Os pesticidas
O processo de secagem, com a redução do teor de água, acaba por aumentar o teor de resíduos de pesticidas presentes na fruta. Além disso, após a secagem é comum o uso da técnica de fumigação para garantir a ausência de pragas nos frutos secos, interrompendo ciclo de insetos que poderiam se desenvolver. Com base nisso, as uvas-passas estão entre as frutas mais contaminadas do mercado, segundo o EWG’s Shopper’s Guide to Pesticides in Produce.
Existem notificações do RASFF citando resíduos dos pesticidas clorpirifós e procimidona acima do lime aceitável, o que evidencia a ocorrência de tal perigo para esse tipo de fruta processada. Além disso, em 24 de novembro desse ano, a Alemanha reportou outro alerta de pesticidas acima dos limites em uvas-passas.
Os mais comuns: perigos físicos
Pequenas surpresas normalmente acompanham as frutas secas, incluindo aqui a uva-passa. Esses perigos podem ser a presença de pedrinhas, fragmentos da planta como galhos e hastes, inclusive insetos mortos. O processo de secagem acaba por deixar as frutas expostas a pragas, como os insetos. O mais comum para uvaspassas são fragmentos de galhos e areia.
Além disso, a infestação por insetos é comum durante o armazenamento da fruta seca. Eles são atraídos pelo alto teor de açúcar, associado ao alto longo período de armazenamento e falhas no programa de controle de pragas do local e na cadeia logística.
Nesta etapa, as condições da cadeia de abastecimento contribuem para o aparecimento ou desenvolvimento de alguns desses perigos, principalmente o armazenamento e distribuição a granel. Isso se deve à exposição ao ambiente, bem como aos instrumentos de manipulação. Isso também se aplica ao armazenamento nos locais de venda ao consumidor final e, até mesmo, em casa.
Relatos de casos
A visibilidade destes casos é maior nos Estados Unidos e Europa, mas não significa que a ocorrência no Brasil é menor. O sistema de alerta da Europa (RASFF), bem como a sistemática definida pelo FDA nos Estados Unidos, garantem a robustez da rastreabilidade e divulgação. Além disso, a Europa possuiu um sistema agressivo de controle de fronteira, com programas de coleta bem administrada com fiscalização.
No Brasil, a maior parte das frutas secas ou desidratadas típicas de Natal, como passas, damasco, figo e tâmara, é importada. No caso das uvas-passas, isso se deve às condições de cultivo das variedades específicas. Assim sendo, a cadeia de distribuição tende a incluir transportes de longo prazo e seus riscos associados, além de incrementar dificuldades na rastreabilidade.
Apesar dos programas de controle de fronteira no Brasil pela VIGIAGRO (MAPA), nem todos os lotes são fiscalizados, havendo margem de risco devido à característica de amostragem e capacidade dos órgãos fiscalizadores na realização de testes, além dos custos a eles relacionados.
Gerenciamento de riscos
Todos esses riscos são gerenciáveis na cadeia de produção e distribuição. Na indústria de alimentos trabalhamos com a aplicação de medidas de controle e monitoramento, a partir de um plano de análise de perigos, os quais podem ser minimizados ou controlados.
Além disso, o processo de fiscalização reforça a importância das indústrias e importadoras da aplicação das medidas de controle em todas as etapas da cadeia de distribuição, evitando perdas de produto e reputação da marca, além do impacto à saúde de seus consumidores.
Mas e agora, estou seguro consumindo o famoso arroz com passas de Natal?
Bem, as uvas-passas têm riscos conhecidos, em especial os relacionados a micotoxinas. As frutas secas exigem controle rigoroso da matéria-prima, do processo de secagem, armazenamento e distribuição. Os órgãos reguladores continuam cumprindo o seu papel de fiscalização nas condições atualmente disponíveis.
Dessa forma, nós, enquanto consumidores, devemos priorizar o uso de marcas reconhecidas por seu padrão de qualidade, de forma a ter maior garantia de que o clima permanecerá festivo após o Natal.
Com isso, me conte aqui: você é do time #compassas ou #forapassas?
Boas festas!
3 min leituraAproxima-se o período de festas de fim de ano, e com ele as polêmicas uvas-passas. Com elas funciona assim: ou se ama ou se odeia. Mas aqui trago uma outra […]