Nada como um bom cafezinho, não é mesmo? Então prepare sua xicrinha e vamos ao artigo.
O cafeeiro (Coffea sp.) é um arbusto da família Rubiaceae e do gênero Coffea L., originário de um local chamado Kaffa nas terras altas da Etiópia na África, local onde os frutos e a planta eram chamados de “bunn” e o arbusto de “bunchum“.
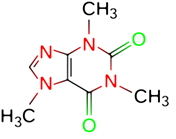
A bebida produzida com o café é feita a partir de suas sementes, após serem torradas e moídas. O pó pode ser filtrado ou não, e a bebida é normalmente servida quente, mas também pode ser fria. Por conter em torno de 40 a 70 mg do alcaloide cafeína (trimetilxantina) a cada 100 mL da bebida, dependendo do método de preparo, o café tem uma ação estimulante, aumenta o estado de alerta e reduz a sensação de fadiga.
Entre as cerca de 103 espécies desse gênero, destacam-se três:
- Coffea arabica– suas variedades mais comuns são a Typica e o Bourbon, que originaram outras cultivares como a Caturra (Brasil e Colômbia), Mundo Novo (Brasil), Tico (América Central), San Ramon (América Central), Blue Mountain (Jamaica) e Sumatra (Indonésia). Dessas ainda se originaram outras como a Catuaí, híbrido do Mundo novo e do Caturra;
- Coffea canephora– sua variedade mais comum é a Robusta, sendo cultivada na África ocidental e central, no sudoeste da Ásia e em algumas regiões do Brasil, em especial no Espírito Santo, onde é conhecida como Conilon;
- Coffea liberica– sua variedade é chamada de Dewevrei, conhecida como Excelsa e é nativa da África, não sendo muito demandada.
Registros históricos de 575 d.C indicam o Iêmen, no atual sudoeste da Ásia, como a primeira região a receber as sementes de café. Lá os árabes dominaram rapidamente a técnica de plantio e preparação e nomearam as plantas de “kaweh” e sua bebida de “kahwah”, que pode ser traduzido como “força”.
Dali o café se espalhou por toda Arábia, porém, existiam várias proibições do consumo de álcool em virtude da religião islâmica. Em Meca, o emir Kha’ir Bey observou vários homens fora da mesquita bebendo o que lhe parecia ser álcool em locais que lembravam tabernas rudimentares. Ele fez perguntas e descobriu que na verdade era uma bebida nova, o café, então proibiu seu consumo naquela cidade, até que relatou sua ação ao sultão no Cairo, que posteriormente ordenou-lhe que revogasse a proibição, afinal não se tratava de uma bebida alcoólica.
Há relatos de que o sufi Baba Budan levou a planta de café do Iêmen para o Estado de Mysore na Índia e o cultivo começou a se espalhar em outras áreas além da Arábia.
Em 1475 uma loja de café foi aberta em Constantinopla, cidade onde a Ásia se encontra com a Europa. Lá foi apelidada de vinho da Arábia e se espalhou pelo mundo, em grande parte, devido às trocas comerciais motivadas pelas grandes navegações e consequentes descobrimentos.
Em sua jornada o café chegou a Java, passou a ser foco do interesse comercial da Companhia da Índias Ocidentais. A partir daí, graças ao dinamismo marítimo holandês, foi introduzido no Novo Mundo, espalhando-se nas Guianas, Martinica, São Domingos, Porto Rico e Cuba.
Já por volta de 1570, o hábito de tomar café foi introduzido em Veneza, sendo proibido aos cristãos, até que o Papa Clemente VIII provou café, gostou do que bebeu, teve clemência e o liberou. Bendito seja ele por isso.
Daí em diante caiu no gosto europeu e em 1652 na Inglaterra foi aberta a primeira casa de café da Europa Ocidental. Cerca de 20 anos depois, a capital francesa Paris também inaugurava sua casa de café. A França foi o País no qual pela primeira foi adicionado açúcar, durante o reinado de Luiz XIV, a quem haviam oferecido um cafeeiro em 1713.
O café passou a fazer parte dos círculos intelectuais europeus, das mesas de discussão política nos famosos cafés de Paris. Foi de certo modo a bebida que “estimulou” o Iluminismo, que culminou na revolução Francesa, afinal, o café é um reconhecido estimulante devido à já citada cafeína, sendo uma bebida perfeita para longas conversas e animadas discussões.

Gravura do século XVIII que mostra Voltaire, Diderot e outros filósofos conversando em um café.
No Brasil o café chegou em 1727 pelas mãos de Francisco de Mello Palheta, um oficial português que trouxe as primeiras mudas provenientes da Guiana Francesa, um presente que recebeu das mãos de Madame D’Orvilliers, esposa do governador de Caiena, e que obviamente, não imaginava no que o presente se tornaria para o Brasil.
Estas mudas foram plantadas no Pará, onde floresceram sem dificuldade. Depois, espalharam-se por todo o País, tornando-se um importante comodities comercial, tanto que tivemos o chamado “ciclo do café” que perdurou por mais de 100 anos, entre 1800 e 1930, no qual a cafeicultura se manteve como a principal atividade econômica do Brasil.
O resultado desta história é que o Brasil produz atualmente cerca de 58,8 milhões de sacas de café por ano (cada saca tem 60 kg), dos quais cerca de 40% ficam para o consumo interno e nos coloca na segunda posição entre os maiores consumidores da bebida em volume. Já numa avaliação per capita, segundo a Embrapa, o consumo brasileiro estimado gira em torno de 6,4 kg/ habitante/ ano. Os 60% restantes do café produzido seguem para exportação, sendo que somos o maior exportador mundial de café, aliás, posto que detemos há mais de 150 anos.
Tabela 1) Ranking dos maiores produtores internacionais de café:
| Ranking | País | Participação total no mercado |
| 1° | Brasil | 38,1 % |
| 2° | Vietnã | 17,8% |
| 3° | Colômbia | 6,7% |
| 4° | Indonésia | 5,6% |
| 5° | Etiópia | 4,8% |
Fonte: USDA, 2023
Como curiosidade, o maior consumidor de café per capita é a Finlândia com 12 kg/ habitante/ ano, depois vem a Noruega com 9,9, Islândia com 9, Dinamarca com 8,7 e Suécia com 8,2, o que mostra que os povos nórdicos realmente apreciam esta bebida. Imagine se ela já existisse nos tempos das invasões vikings.
Do café produzido no Brasil, o arábica corresponde a cerca de 64% e conilon a 36%. De uma forma geral, o café arábica é mais complexo, encorpado, suave e, por isso, é considerado um café mais fino, enquanto o conilon ou robusta é considerado um café mais neutro, com um leve amargor, porém possui mais substâncias solúveis (açúcares e cafeína) com grande aceitação no mercado americano e europeu, sendo muito valorizado para composição de blends e pela indústria de café instantâneo.

Mas o café que você toma é café mesmo ou impurezas bem torradinhas?
O Departamento de Inspeção de Produtos de Origem Vegetal da Secretaria de Defesa Agropecuária do MAPA (Ministério da Agricultura e Pecuária), entre os dias 18 e 28 de março deste ano, numa ação de fiscalização denominada “Operação Valoriza”, coletou 168 amostras de café torrado e moído por todo o Brasil para realizar análises.
O resultado desta fiscalização indicou que 14 marcas continham matérias estranhas e impurezas ou elementos estranhos acima dos limites permitidos pela Portaria da Secretaria de Defesa Agropecuária – SDA Nº 570, de 9 de maio de 2022, que dispõe sobre requisitos de identidade e qualidade, amostragem, modo de apresentação e a marcação ou rotulagem, nos aspectos referentes à classificação do café torrado e moído.
Tabela 2) Marcas que foram identificadas como impróprias:

Fonte: MAPA, 2024
Este produtos que foram considerados impróprios para consumo deverão ser recolhidos pelas empresas responsáveis, pois o café identificado com este tipo de “material estranho” configura adulteração, fraude ou falsificação. Em alguns casos, pode até significar riscos à saúde pública.
A orientação aos consumidores é que não consumam estes produtos, podendo solicitar sua substituição nos locais onde eles foram adquiridos conforme determina o Código de Defesa do Consumidor.
Normalmente os materiais estranhos mais comuns no café são os defeitos que ao longo do processo de beneficiamento devem ser separados e eliminados, como cascas do café, pedaços da planta como pequenos galhos/ caules, folhas, grãos chochos ou brocados. Porém, também podem prover de falhas de BPF (Boas Práticas de Fabricação) como ácaros, larvas, insetos e seus fragmentos, pelos de roedores, bárbulas etc.

Tais problemas podem ser gerados devido à incompetência no controle dos processos. Porém, mais comumente e infelizmente, ocorrem por má fé, fazendo-se uso da adição do residual de defeitos que deveriam ser descartados ao café que receberá uma torra excessiva para disfarçar estes problemas. Depois este café costuma ser comercializado sob o nome de “extra forte”, mas de forte não tem nada, apenas material carbonizado que gera uma cor muito escura e um sabor residual amargo.
Quando um produtor permite um número de defeitos ou materiais estranhos acima do permitido, isso significa na prática que ele está fraudando o consumidor, pois está vendendo sujidades torradas como se fosse café, em busca de vantagens econômicas.
Um bom café, ou seja, com grãos selecionados e baixa impureza, não requer torra excessiva. Sua cor é um castanho escuro de tons levemente avermelhados e intensas notas sensoriais, pois com a torra cuidadosa são conservados os óleos essenciais que remetem a nuances aromáticos de caramelo, chocolate, nozes, baunilha e mel. Justamente por isso, um bom café dispensa ser adoçado.
O lado bom é que apesar dos maus produtores, os bons são a maioria, e justamente por isso, o Brasil se destaca há tanto tempo no mercado internacional desta bebida, e a cada dia surgem melhores cafés. O fator qualidade tem se sobreposto em relação ao volume para muitos produtores, e cada vez mais se valoriza o terroir de sua produção, plena seleção de grãos, cuidados especiais de torra e combinações utilizando-se o melhor do café conilon que se destaca no Espírito Santo e do arábica que se destaca em Minas Gerais.
Tabela 3) Maiores Estados produtores de café no Brasil:
| Ranking | Estado | Participação total no mercado |
| 1° | Minas Gerais | 50,8 % |
| 2 ° | Espírito Santo | 25,3 % |
| 3 ° | São Paulo | 9,0 % |
| 4 ° | Bahia | 6,7 % |
| 5 ° | Rondônia | 5,7 % |
Fonte: Sumário Executivo Café, 2023
Na prevenção de fraudes em alimentos e bebidas a informação ao consumidor é uma arma valiosa, e claro, ações de fiscalização para coibir práticas fraudulentas para que as tornem inviáveis economicamente são fundamentais.
Termino aqui meu artigo e vou tomar mais uma xícara de café! Deixe seu comentário, ele é muito importante para nós.
Leia também sobre café:
- Sujidades leves em café torrado – Embrapa
- Os defeitos dos grãos e café e suas principais causas – Rehagro
- Mapa divulga lista de marcas e lotes de café torrado impróprios para consumo – MAPA
- Quais são os 5 maiores produtores de café no mundo? Brasil se destaca! – Agroadvance
- Consumo interno de café no Brasil – Embrapa
- Degradação da Ocratoxina (OTA) no café por emprego de temperatura
- PROTESTE detecta quase o triplo de Ocratoxina A e seis vezes mais fragmentos de insetos em Café
Leia também sobre fraudes em alimentos e bebidas:
- Fraudes históricas no vinho
- Dicas para prevenir a compra de azeite de oliva fraudado
- Aprenda a escolher um bacalhau de verdade
- Cachaça boa é a cachaça segura
- Boas práticas para garantir qualidade e segurança da pimenta-do-reino
7 min leituraNada como um bom cafezinho, não é mesmo? Então prepare sua xicrinha e vamos ao artigo. O cafeeiro (Coffea sp.) é um arbusto da família Rubiaceae e do gênero Coffea L., […]