A doença de Parkinson é o segundo transtorno neurodegenerativo mais comum após a doença de Alzheimer. Embora a causa exata seja incerta para a maioria das pessoas, há evidências emergentes que vinculam a doença a fatores ambientais, incluindo a exposição a bolores e leveduras.
Um exemplo ilustrativo é o estudo realizado por Arati Inamdar e Joan Bennett, da Rutgers University, publicado em 2013. Nessa pesquisa, os cientistas utilizaram moscas de fruta para investigar o impacto do 1-octen-3-ol, também conhecido como “álcool de cogumelo”, um composto volátil liberado por bolores. Os resultados, divulgados nos Anais da Academia Nacional de Ciências, indicam que este composto pode comprometer a dopamina e desencadear sintomas característicos da doença de Parkinson, sublinhando a possível conexão entre compostos biológicos e a patologia.
No Brasil, uma pesquisa relevante conduzida por Dionísio Pedro Amorim Neto na Unicamp (2024) explora similarmente a relação entre fungos e leveduras presentes na microbiota intestinal e a doença de Parkinson. Esse estudo, que revisou mais de cem artigos científicos, foca a influência desses microrganismos ou de seus metabólitos secundários na origem e progressão da doença. Os resultados apontam que tais organismos podem tanto proteger quanto induzir sintomas da doença. Amorim sugere que os metabólitos dos microrganismos intestinais podem alcançar o cérebro pela corrente sanguínea ou afetar as células do epitélio intestinal, que por sua vez podem influenciar os neurônios. Outra hipótese levantada é que as células neuroendócrinas do intestino poderiam interagir com o nervo vago e desencadear a patologia. Embora os estudos indiquem que certas espécies de Candida são mais abundantes nos intestinos de pacientes com Parkinson, e outras leveduras probióticas parecem ter efeitos benéficos, ainda existe uma lacuna significativa no entendimento da interação específica dos fungos com a doença, um tema que Amorim pretende explorar durante seu doutorado.
Esses estudos destacam a importância de garantir a segurança dos alimentos, pois microrganismos como bolores e leveduras podem estar associados a doenças cujos efeitos ainda não compreendemos completamente.
Nesse cenário, enfatiza-se a prevenção da contaminação cruzada, exemplificando o monitoramento ambiental como uma ferramenta eficaz. Manter um ambiente livre de agentes patogênicos ou tóxicos é crucial, e esse programa destaca a necessidade de adotar medidas rigorosas de higiene e vigilância constante durante o processamento de alimentos.
Um plano de monitoramento ambiental eficaz visa principalmente evitar a contaminação cruzada entre o ambiente (ar, equipamentos, colaboradores, etc.) e o produto. Ao combinar a monitorização dos alimentos e do ambiente de produção, é possível assegurar a qualidade e segurança dos alimentos. Para um plano de monitoramento eficaz, é necessária uma estruturação como a mostrada no quadro abaixo.
| Etapa | Descrição Completa |
| 1. Estruturação do Plano de Monitoramento | A equipe responsável deve ser multidisciplinar e ter treinamento em segurança de alimentos, com conhecimento do processo produtivo. |
| 2. Treinamento de Equipe | Equipe treinada em patógenos alimentares, avaliação de risco de patógenos alimentares e testes microbiológicos, fomentando uma cultura de segurança de alimentos. |
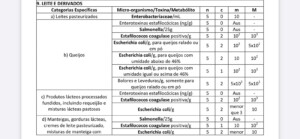
| 3. Microrganismos a serem avaliados | Para a adequada definição de microrganismos a serem monitorados em conformidade com o sistema de Análise de Perigos e Pontos Críticos de Controle (APPCC), é essencial considerar as condições de limpeza e as boas práticas de fabricação vigentes. Esta etapa envolve uma análise criteriosa das características dos microrganismos, tais como: a) Identificação dos microrganismos mais comuns no processo específico. b) Avaliação de suas condições para serem classificados como patogênicos, deteriorantes ou indicadores. c) Determinação da capacidade de formação de biofilme pelos microrganismos. d) Necessidade de utilização de inibidores de sanitizantes. eCondições existentes que permitam o crescimento do microrganismo após a coleta ou possibilidade de que este fique injuriado.Além disso, é imperativo realizar uma análise de risco que considere a probabilidade de ocorrência, a severidade e o risco associado a cada microrganismo. Neste contexto, destacam-se patógenos como Salmonella spp., Cronobacter spp., e Listeria monocytogenes, bem como indicadores e deteriorantes como Enterobactérias, Bolores e leveduras, e Aeróbios Mesófilos. |
| 4. Estruturação do zoneamento ambiental | Descrição das zonas de monitoramento: Zona 01 – com superfícies de contato direto com o produto; Zona 02 – com superfícies sem contato direto mas próximas; Zona 03 – com áreas sem contato direto e não próximas; Zona 04 – com áreas distantes do processamento.
Observação: Na zona 1 não incluir patógeno, somente indicador, caso tenha patógeno somente liberar produto após resultado de análise). Foco em bactéria indicador. |
| 5. Definição do plano de amostragem | Identificação de áreas vulneráveis à contaminação, usando métodos como testes microbiológicos (placas de Petri, swabs, esponjas), métodos moleculares (PCR) e sensoriamento remoto ou coleta diferenciada do ar. |
| 6. Ações Preventivas | Implementação de controle de umidade e temperatura, ventilação adequada e rotinas de limpeza e sanitização. |
| 7. Análise dos resultados | Análise de tendências por ponto avaliado para identificar áreas que necessitam de atenção, revisão e expansão do plano conforme necessário, com atenção especial à precisão das unidades de medida. |
Além das recomendações sobre monitoramento ambiental, você pode encontrar artigos como material complementar em nosso blog, incluindo:
- Elaborando um plano de monitoramento ambiental
- Quais microrganismos devo considerar no Plano de Monitoramento Ambiental?
- Tradução: Guia de Monitoramento Ambiental FSSC 22000
- Biologia molecular e o monitoramento ambiental na nova era da microbiologia da indústria de alimentos
- Monitoramento ambiental de patógenos (PEM) para alimentos de baixa atividade de água
- Publicação de Guia para Programa de Monitoramento Ambiental, com indicadores e níveis aceitáveis;
- Como transformar dados em informações no monitoramento ambiental da indústria de alimentos?
3 min leituraA doença de Parkinson é o segundo transtorno neurodegenerativo mais comum após a doença de Alzheimer. Embora a causa exata seja incerta para a maioria das pessoas, há evidências emergentes […]