7 min leituraOs perigos radiológicos em alimentos provêm de radioisótopos, também chamados de radionuclídeos. São átomos sujeitos ao processo de decaimento radioativo, liberando assim radioatividade através de partículas alfa, beta e gama. Eventualmente, podem chegar à cadeia produtiva de alimentos, expondo as pessoas à contaminação e gerando efeitos adversos à saúde, cuja gravidade dependerá especificamente do radioisótopo e do grau de radiação ao qual um indivíduo foi exposto.
No entanto, segundo a Organização Mundial da Saúde (OMS), os perigos radiológicos são incomuns na cadeia produtiva de alimentos. A grande questão é que quando ocorrem, podem representar um risco de elevada significância, principalmente se a exposição ao risco for prolongada ao longo do tempo.
A ingestão de alimentos ou água com radioisótopos leva a uma contaminação interna na qual o material radioativo irá se depositar no organismo, podendo ser transportado para vários locais, tais como a medula óssea, onde continua a emitir radiação, aumentando a exposição da pessoa à radiação, até ser removido ou emitir toda sua energia (desintegração).
A contaminação interna com radioisótopos é mais difícil de remover do que a contaminação externa.
O consumo de alimentos contaminados com radioisótopos aumenta a quantidade de radioatividade a qual a pessoa é exposta, o que pode provocar efeitos agudos como vermelhidão da pele (eritemas), queda de cabelo e síndrome de radiação aguda, que inclui sintomas iniciais como náuseas, vômitos, dor de cabeça e diarreia. Com o tempo, pode chegar a uma perda de apetite, fadiga e possivelmente convulsões e coma. Em alguns casos, pode provocar doenças graves, inclusive alguns tipos de câncer, como na tireoide e leucemia.
A maioria dos elementos radioativos naturais tem sua origem na crosta terrestre como o Potássio-40 (K-40), Urânio-238 (U-238) e Tório-232 (Th-232), que são elementos radioativos primitivos, ou seja, estão presentes desde a formação da Terra há cerca de 4,6 bilhões de anos.
A população mundial está exposta diariamente à radiação natural, que vem do espaço através dos raios cósmicos e de materiais radioativos que ocorrem no solo, na água e no ar, quase sempre, em quantidades ínfimas e inócuas à saúde.
Porém, a radiação pode ocorrer também devido aos efeitos antrópicos, tendo como exemplos os acidentes nucleares ocorridos em Chernobyl, na Ucrânia, em 1986, quando esta pertencia à URSS (União das Repúblicas Socialistas Soviéticas) e em Fukushima no Japão em 2011. Em consequência, a superfície de alimentos como cereais, frutas e legumes ou destinados para alimentação de animais para leite ou corte, pode se tornar radioativa devido à deposição de poeira com radioisótopos ou da água da chuva contaminada.
Além do efeito imediato, os locais onde houve exposição aos elementos radioativos se tornarão áreas de risco, uma vez que o solo ficará contaminado. Com o tempo, a radioatividade também poderá ser detectada nos alimentos porque os radioisótopos do solo serão absorvidos pelas plantas, e em seguida, pelos animais que se alimentam delas, chegando à carne, ao leite e derivados, portanto, à cadeia alimentar humana.
O Césio-137 tem um período de semidesintegração de 30 anos, e por isso afeta áreas agricultáveis durante décadas.
Como exemplo, ainda citando o fatídico acidente de Chernobyl, a nuvem de poeira radioativa cujos principais radioisótopos produzidos na reação de fissão (divisão) nuclear do Urânio-235 (combustível nuclear do reator) foram o Iodo-131, Césio-137, Césio-134 e o Estrôncio-90, varreu a Europa e causou a precipitação destes radioisótopos em diversos países da Europa e da Ásia. Isto é mostrado no mapa a seguir, com graves perturbações na produção e no comércio de produtos alimentícios.
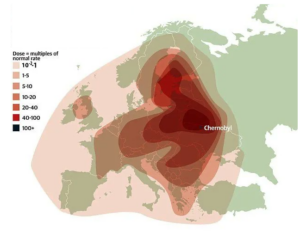
Mapa com a nuvem de radiação que envolveu a Europa durante o desastre de Chernobyl em 1986.
Na ocasião do acidente em Chernobyl, o Brasil havia importado carne bovina e leite de países que estavam dentro do raio atingido pela poeira radioativa, como a Alemanha, Holanda e França. Descobriu-se mais tarde que estes alimentos estavam contaminados com os radioisótopos Césio-137 e Césio-134, potencialmente cancerígenos.

Jornal Correio do Povo de 21 de janeiro de 1988.
Já no acidente mais recente em Fukushima não houve impactos no Brasil, uma vez que não somos um importador habitual de alimentos do Japão. No entanto, naquele país diversos alimentos como carne, chá, cogumelos e verduras cultivados nas proximidades da região de Fukushima, foram identificados com níveis de radioatividade acima do permitido para o consumo, inclusive arroz, alimento tradicional da culinária japonesa, numa fazenda a 60 quilômetros da instalação nuclear.
A experiência em Fukushima mostrou existir dificuldades para rastrear a radiação espalhada pela chuva e o vento, sendo que governos locais em áreas rurais montaram centros de teste para evitar a distribuição de produtos contaminados e a própria população começou a medir radiação por conta própria, usando aparelhos simples.

Jornal Hoje, G1 de 19 de março de 2011.
Seja por origem natural ou antrópica, a água potável ou mineral pode absorver a radioatividade, e assim, contaminar peixes e frutos do mar. Por isso, estima-se que os frutos do mar são os alimentos com radiação natural mais concentrada, e, também, com grande probabilidade de exposição aos acidentes nucleares.

CNN Brasil de 26 de julho de 2023.
Por isso, na análise de perigos radiológicos em alimentos num plano de HACCP, há que se considerar a probabilidade do risco em cada região produtora e em cada alimento específico, levando em consideração a rastreabilidade de sua origem para poder avaliar o histórico de acidentes nucleares na região (lembrando que partículas radioativas podem permanecer ativas por décadas), a proximidade a locais de guarda de lixo nuclear, assim como áreas geográficas onde existam depósitos naturais de minerais radioativos como os uraníferos ou de tório.
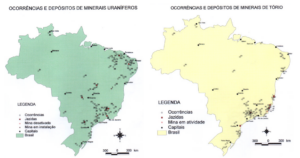
Localição georgráfica no Brasil de jazidas de minérios radioativos.
No entanto, apelando para a obviedade, veja que um peixe proveniente do mar do Japão próximo à região costeira de Fukushima, terá uma probabilidade de contaminação radioativa muito maior que um outro que foi pescado na costa brasileira. Analogamente, grãos provenientes da Ucrânia, onde ocorreu o acidente de Chernobyl, terão uma probabilidade maior do que aqueles cultivados no cerrado brasileiro.
Não há no Brasil uma legislação ou referências específicas para níveis máximos permitidos de contaminação radioativa em alimentos, no entanto, há para água destinada ao consumo humano.
A Portaria GM/ MS Nº 888 do Ministério da Saúde, no Art. 37 dita que “os níveis de triagem usados na avaliação da potabilidade da água, do ponto de vista radiológico, são os valores de concentração de atividade que não excedam 0,5 Bq/L para atividade alfa total e 1,0 Bq/L para beta total, portaria esta que foi analisada no artigo “Análise da nova Portaria MS 888/21 sobre controle e vigilância da água para consumo humano“.
Monitorar água, em especial proveniente de poços artesianos em regiões onde há probabilidade natural de radioisótopos, é muito relevante, e logicamente, caso os níveis radiológicos ultrapassem o que está definido na legislação, o consumo deve ser vetado.
Neste tema é relevante um esclarecimento sobre irradiação, que não deve ser confundida com contaminação radiológica
Numa contaminação radioativa, como visto, há presença de um isótopo radioativo indesejável que é capaz de emitir radiação (alfa, beta e gama) de forma espontânea a partir de seus núcleos instáveis e, assim, causar danos à saúde. Porém, em alimentos que passaram por um processo de irradiação não, pois trata-se da exposição deste alimento à radiação, porém, sem contato direto com os elementos radioativos.
A tecnologia de irradiação de alimentos foi aprovada pela Organização das Nações Unidas para a Agricultura e Alimentação (FAO) como segura e é utilizada em cerca de 50 países. Estima-se que o volume de alimentos tratados em todo o mundo por esta tecnologia exceda 500 mil toneladas anualmente, sendo um método eficaz para melhorar a qualidade de produtos alimentícios reduzindo cargas microbianas e aumentando a shelf life.
Esse processo é bastante utilizado em frutas frescas, grãos e vegetais para prevenir o brotamento, retardar a maturação e aumentar o tempo de conservação, uma vez que os alimentos são submetidos a uma quantidade minuciosamente controlada e precisa de radiação. Sugiro neste tema a leitura dos artigos:
- Radioatividade do bem: entenda a técnica de irradiação de alimentos
- Por uma cultura de segurança de alimentos baseada na ciência: mitos sobre alimentos processados e irradiação
A irradiação não faz com que o alimento se torne radioativo, não compromete a qualidade nutricional e não altera sabor, textura ou aparência do alimento. Além disso, o uso de radiação ionizante é uma opção com menor impacto ambiental, pois não deixa resíduos.
Um alimento irradiado praticamente não sofre qualquer alteração física ou organoléptica, por isso é muito difícil dizer se o alimento foi ou não irradiado.
No Brasil, a regulamentação sobre alimentos irradiados é definida pelo Decreto nº 72.718, de 29 de agosto de 1973, que estabelece normas gerais sobre irradiação de alimentos e pela Resolução ANVISA – RDC nº 21, de 26 de janeiro de 2001, que aprovou o Regulamento Técnico para Irradiação de Alimentos, estabelecendo os requisitos gerais para o uso da irradiação de alimentos com vistas à qualidade sanitária do produto final. Lembramos que deve sempre haver transparência ao consumidor, pois nos rótulos dos alimentos que passaram por este processo deve constar a frase “alimento tratado por processo de irradiação”, como visto no artigo “Anvisa entende que alimento que passa por raios X deve ser rotulado como irradiado“.

Logomarca utilizada para alimentos irradiados.
Espero que o artigo tenha ajudado a perceber que o tema dos riscos radiológicos não é um bicho de sete cabeças, mas que precisa ser visto com atenção, considerando a necessidade de uma boa análise de riscos em relação à probabilidade de contaminação e rastreabilidade da água e insumos utilizados na cadeia produtiva de alimentos.
Deixe sua opinião, complemente com sua experiência e seu conhecimento, isso é muito importante para nós!
Leia também:
Irradiação e perigos radiológicos em alimentos
FDA permite o uso de irradiação em crustáceos para controle de patógenos de origem alimentar
Perigos radiológicos foram levantados no seu plano HACCP?
Visualização da postagem 5.054
7 min leituraOs perigos radiológicos em alimentos provêm de radioisótopos, também chamados de radionuclídeos. São átomos sujeitos ao processo de decaimento radioativo, liberando assim radioatividade através de partículas alfa, beta e gama. […]