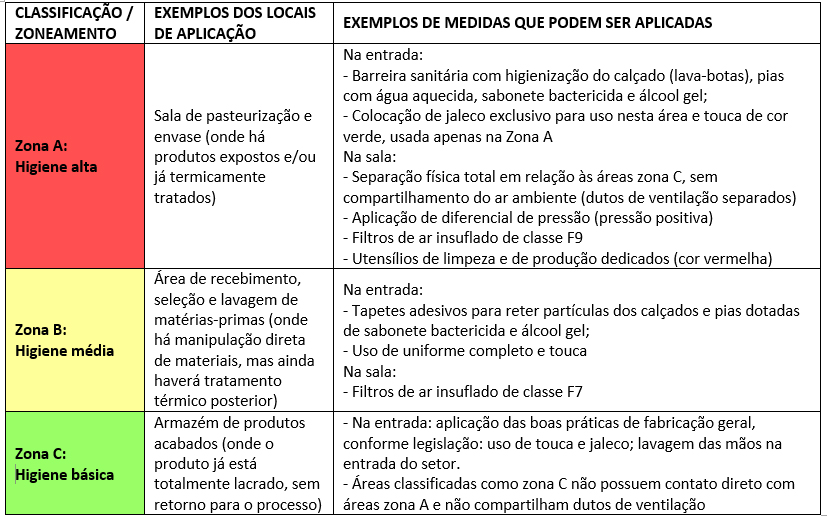
Recentemente publiquei uma matéria sobre como passar em uma auditoria de certificação. Como já sabemos, não há uma fórmula mágica, mas quais seriam as decisões práticas que precisamos tomar / articular para poder ter uma auditoria o mais tranquila possível?
1 – Prazos
Vamos começar pensando em prazo de auditoria de certificação. A organização já definiu o prazo limite? Muitas vezes este prazo está atrelado a algum objetivo da organização (como realizar naquele ano calendário ou ano fiscal…. ou num determinado semestre daquele ano, por exemplo).
Se este for o caso, em primeiro lugar certifique-se de que o organismo certificador tem disponibilidade de agenda para cumprir este prazo. É comum que o último trimestre do ano seja bem disputado. Muitas empresas definem as metas anuais já considerando a certificação, o que deixa as agendas dos organismos certificadores e dos auditores bem disputada.
A partir daí, pense em fazer uma contagem regressiva. Se a data já está definida (ou a semana), considere realizar a auditoria interna com no mínimo 3 a 4 meses de antecedência desta data. Assim a equipe terá tempo hábil para tratar os possíveis desvios identificados na auditoria interna antes da auditoria de certificação.
Aqui cabem uns parênteses para as ações que necessitam de investimentos. Estas precisam ser mapeadas com muito mais antecedência, pois precisam ser planejadas. Algumas vezes pequenos investimentos são possíveis de realizar em pouco tempo, mas conte com imprevistos. Eles podem acontecer (e em geral acontecem e podem comprometer o prazo inicialmente planejado).
2 – Auditoria Interna
Uma boa auditoria interna serve tanto para identificar as oportunidades do SGSA quanto para fazer um simulado com a equipe que será auditada durante o processo de certificação.
Esta é a etapa de sermos muito verdadeiros. Qualquer oportunidade que vier a ser identificada nesta fase pode ser tratada sem que tenham surpresas desagradáveis envolvidas. Isto não significa que eliminamos o risco de uma não conformidade. Mas há grandes chances de que as falhas significativas (potenciais não conformidades maiores) sejam vistas nesta etapa.
A auditoria interna pode ser realizada pela equipe interna ou por uma consultoria especializada. Pontos importantes na seleção da opção:
Equipe interna: garanta que a equipe consiga avaliar os requisitos na profundidade adequada para verificar a conformidade das exigências em cada item da norma. Tanto na parte documental quanto na parte estrutural e registros. É comum que auditores internos sem experiência naveguem de forma superficial nos requisitos e não consigam avaliar adequadamente o atendimento ou em algumas situações não perceber que há uma falha sistêmica no assunto avaliado;
- Consultoria especializada: a consultoria deve ser especializada em sistema de gestão de segurança de alimentos. Apesar de as normas acreditadas terem muitos assuntos “comuns”, é fundamental que a auditoria seja realizada por especialistas para avaliar adequadamente o levantamento de perigos, as medidas de controle, os pré-requisitos, etc.. Então peça referências, se for o caso converse com outros clientes da consultoria, avalie o curriculum do auditor que será designado para o trabalho.
3 – Pós Auditoria Interna
Bom….. depois da auditoria interna vem a etapa de “mão na massa”…. claro que as equipes já estavam trabalhando para a implementação do SGSA, e principalmente a equipe de segurança de alimentos (ESA), mas agora é aquele “gás final”…. kkkk.
Elaborar planos de ação consistentes nesta fase é imprescindível para que os GAPs sejam eliminados e que a auditoria externa seja mais tranquila. Caprichem nas investigações de causa, na elaboração dos planos de ação e seja consciente com os prazos para execução das ações. As ações devem ser executadas antes da auditoria externa (ou a maioria delas).
4 – Pré Auditoria Externa
É comum que os auditados fiquem nervosos durante a auditoria externa. Então vale a pena pensar em fazer um exercício adicional à auditoria interna. Esta não é uma etapa obrigatória, aqui o intuito é fazer com que os auditados sintam-se um pouco mais confiantes para a auditoria externa. Isso pode se aplicar à ESA, ao pessoal diretamente envolvido nas principais operações do processo produtivo, às pessoas responsáveis pelo controle de PCCs, terceiros e prestadores de serviço chave da organização (equipe de limpeza, por exemplo), entre outros.
Também é viável criar uma lista de verificação dos pontos críticos que estão em andamento para um acompanhamento periódico (semanal, e perto da auditoria pode-se pensar em fazê-lo a cada dois dias). Nesta lista considerem as ações de tarefas que estavam em andamento durante a implementação do SGSA, acompanhamento final das obras de infraestrutura que ainda estiverem em andamento, ações derivadas dos planos de ações corretivas da auditoria interna.
5 – Auditoria Externa
Como falamos lá no começo é importante garantir a agenda da auditoria externa com certa antecedência.
A auditoria de certificação é composta de duas fases. Na primeira é basicamente uma avaliação da documentação da organização, uma avaliação prévia das instalações, mas pouco se deve exercitar os controles operacionais ou entrevistas com a operação como um todo. O objetivo aqui é avaliar o requisito 7 da ISO22000:2006 basicamente. Outros pontos podem ser verificados, mas de forma um pouco mais superficial.
Se for o caso, na fase I pode-se recomendar postergar a auditoria fase II. Dependendo das oportunidades e complexidades encontradas neste momento.
Na fase II será acompanhado o desdobramento dos planos de ação identificados na fase I e uma avaliação mais profunda de todos os requisitos da norma, entrevistas com colaboradores, visitas às áreas, avaliação da documentação, etc.
Auditorias de recertificação contemplam somente a fase II, pois se entende que a avaliação da documentação ocorreu na certificação e ao longo das auditorias de manutenção do ciclo de 3 anos.
6 – O resultado e o pós-auditoria externa
O resultado da auditoria externa é mensurado em “recomendado” ou “não recomendado”. A recomendação não depende do número de não conformidades identificadas, e sim da complexidade destas não conformidades (observações, não conformidades menores ou não conformidades maiores).
Na fase final da auditoria externa, os planos de ação das não conformidades já devem estar estabelecidos, com suas devidas análises de causa feitas.
Bem…. não é uma fórmula mágica, mas é quase uma receitinha de bolo…. Então agora é só por pra assar…..
4 min leituraRecentemente publiquei uma matéria sobre como passar em uma auditoria de certificação. Como já sabemos, não há uma fórmula mágica, mas quais seriam as decisões práticas que precisamos tomar / […]