Hoje dou continuidade à série de posts sobre o evento IFS FOCUS DAY 2024, realizado em São Paulo, em 26 de setembro de 2024. Na ocasião, o Prof. Dr. Romeu Cantusio Neto abordou o Plano de Segurança da Água e destacou a importância de ir além dos requisitos normativos. Como a água muda constantemente suas características, é essencial adotar uma avaliação de risco que abranja desde a qualidade e segurança dos alimentos até a gestão de crises e emergências por escassez hídrica.
1. O papel da água na indústria de alimentos e os riscos associados
Dr. Romeu enfatizou que a água é frequentemente negligenciada na indústria de alimentos, mesmo sendo uma matéria-prima essencial com diferentes fontes de captação e origem. Dados alarmantes demonstram a relevância do tema:
- 13% da população mundial não tem acesso à água potável.
- 1,5 milhão de crianças morrem anualmente devido a doenças de transmissão hídrica.
- No Brasil, apenas 55,8% da população tem acesso a saneamento adequado.
Principais fontes de contaminação da água:
- Descargas industriais e urbanas: efluentes lançados diretamente em mananciais comprometem a qualidade da água.
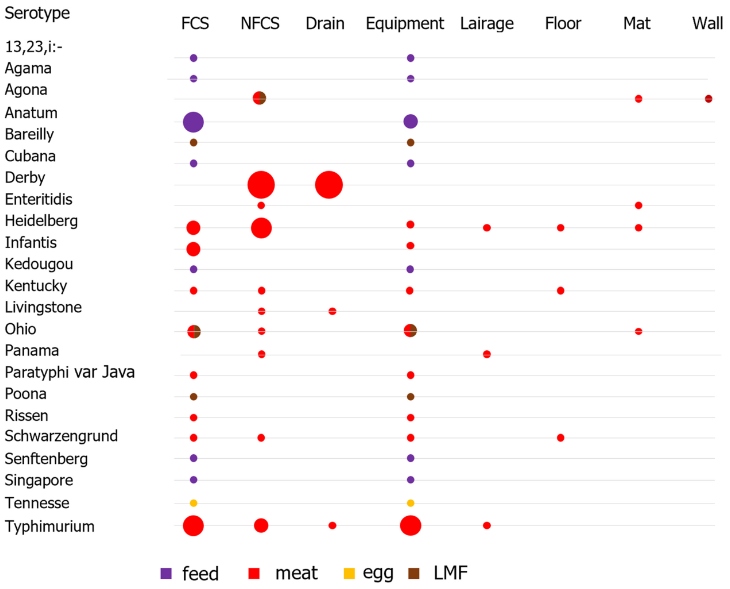
- Patógenos biológicos: protozoários como Cryptosporidium spp. e Giardia spp., além de bactérias resistentes, estão cada vez mais presentes.
- Resíduos químicos e fármacos: substâncias como microplásticos e resíduos farmacêuticos vêm sendo detectadas em fontes de abastecimento.
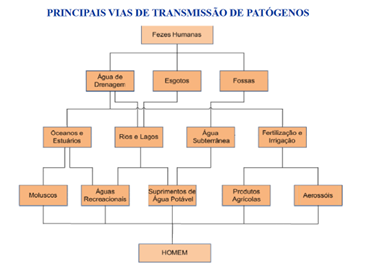
A transmissão de patógenos ocorre por diversas vias, exigindo uma abordagem além dos parâmetros mínimos de qualidade da água e focada na gestão de risco eficiente. Um exemplo crítico são os aerossóis gerados em sistemas de resfriamento, como as torres de resfriamento. A falta de avaliação adequada pode resultar em surtos de Legionella, um microrganismo que forma biofilmes, dificultando seu controle e muitas vezes não sendo considerado no plano HACCP. A prevenção deve priorizar monitoramento contínuo e estratégias eficazes de controle para minimizar os riscos antes que a contaminação ocorra.
2. O Plano de Segurança da Água (PSA) como estratégia preventiva de Gestão de Risco
Diferente das abordagens tradicionais de monitoramento reativo, o PSA propõe um modelo proativo, identificando e priorizando riscos potenciais ao longo de toda a cadeia de abastecimento. O plano se baseia em três pilares fundamentais:
ELIMINAR – reduzir a contaminação durante o tratamento da água.
MINIMIZAR – mitigar a presença de contaminantes na fonte de captação.
PREVENIR – evitar a recontaminação no armazenamento e distribuição.
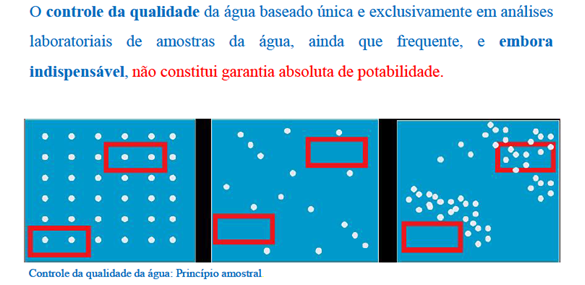
O controle laboratorial pontual e simples não garante a potabilidade da água, pois não capta suas variações contínuas. A qualidade da água muda constantemente, tornando necessário um monitoramento eficaz em diversos pontos do processo (gestão contínua e estruturada)
A dosagem de cloro é fundamental, mas como garantir sua eficácia ao longo do percurso? O controle na saída e pós-cloração é comum, mas e o meio do trajeto? A formação de biofilmes pode passar despercebida, aumentando riscos.
Tratar a água apenas com base na Portaria 888 é o mínimo exigido, mas não é suficiente. O PSA deve ser continuamente aprimorado para garantir segurança e conformidade.
Outro ponto crítico é a falta de tempo de contato adequado do cloro, comprometendo sua eficácia e não garantindo a desinfecção completa (conforme descrito no Anexo da Portaria 888/2021). Na indústria, além da caixa d’água, existem ramificações nas linhas de distribuição, sendo que algumas puxam mais água do que outras. Como garantir que, nas linhas de menor vazão, a água não ficou estagnada e perdeu sua qualidade? E, nas linhas de maior vazão, como assegurar que o tempo de permanência do cloro foi suficiente para uma desinfecção eficaz?
Além disso, diferentes usos da água exigem níveis específicos de preservação – como o consumo humano e a higienização das mãos, especialmente em locais críticos.
Outro fator importante é que o risco da água nem sempre está dentro do sistema, mas também fora dele. Por isso, é essencial uma gestão eficiente da bacia hidrográfica:
Qual a origem da sua água?
Como está o lençol freático do seu poço?
Sua localização geográfica influencia na qualidade do recurso hídrico utilizado?
3. Identificação e classificação de riscos na indústria de alimentos
O controle da qualidade da água na indústria de alimentos deve seguir uma metodologia rigorosa de avaliação de riscos, semelhante à aplicada no APPCC (Análise de Perigos e Pontos Críticos de Controle). O PSA utiliza um sistema de classificação de riscos baseado em critérios de impacto à saúde pública, sendo um plano de fundo para gestão de risco.
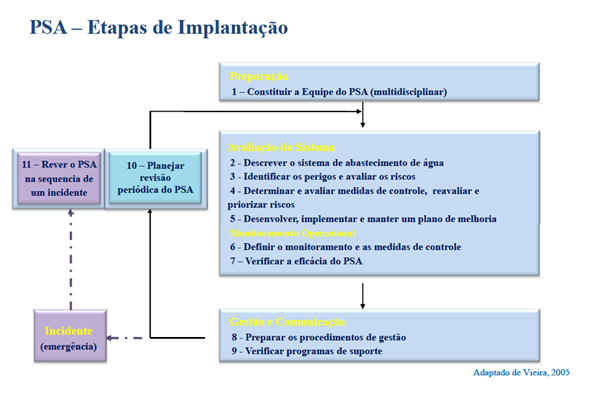
O Brasil, por ser um país de grande extensão territorial, apresenta diferentes condições hidrogeológicas. Cada indústria, localidade e cidade tem suas peculiaridades e características quanto às fontes de abastecimento. Nós estamos vivendo processo crítico pois temos muito pouca água disponível e potável, e a água que temos, muitas vezes pode estar contaminada por substâncias tóxicas ou organismos patogênicos.
Além da escassez, a qualidade da água também está ameaçada pela presença de contaminantes microbiológicos, resíduos de fármacos, hormônios e microplásticos, que os sistemas convencionais nem sempre conseguem remover.
Diante desse cenário, torna-se essencial a implementação de planos de contingência para emergências de falta de água, considerando fontes alternativas.
Dr. Romeu mencionou a impossibilidade atual de se elaborar uma matriz de risco quantitativa, sendo mais apropriada a matriz qualitativa, com base em guias como o do PAS (Plano de Segurança da Água) e da WHO (World Health Organization) que contempla exemplos práticos e passo a passo para elaboração da gestão de risco da água.
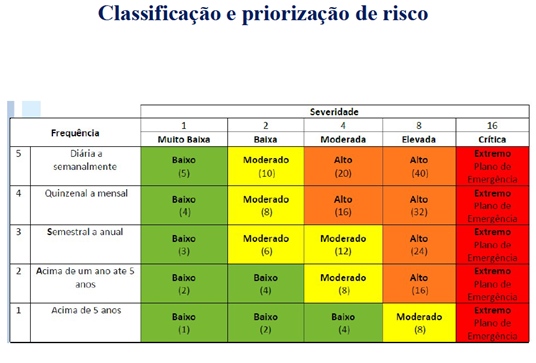
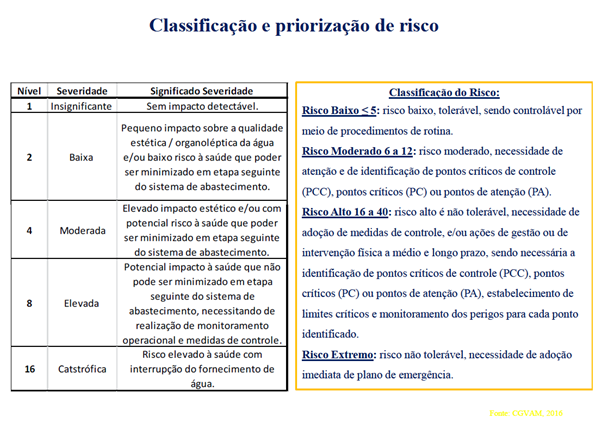

4. O impacto das mudanças climáticas na segurança hídrica e a responsabilidade da indústria
As mudanças climáticas agravam a escassez de água potável, intensificando a concorrência pelo recurso. Um exemplo recente ocorreu no Espírito Santo, onde a vazão do Rio Cricaré diminuiu tanto que, em vez de o rio desaguar no mar, a água salgada está invadindo o rio. O aumento da salinidade forçou a interrupção da captação, comprometendo o abastecimento da população.
A legislação atual estabelece parâmetros mínimos de qualidade da água e seu cumprimento e entendimento é básico, para avançar e aprofundar a gestão de riscos das fontes de captação. Para garantir segurança hídrica, é essencial conhecer a origem da água utilizada.
Além disso, a responsabilidade pela gestão sustentável da água também passa pela indústria, que deve estar alinhada ao Objetivo de Desenvolvimento Sustentável (ODS) 6 da ONU – que visa assegurar a disponibilidade e gestão sustentável da água.
Além disso, a indústria também deve estar alinhada ao ODS 17 da ONU, que visa fortalecer parcerias globais para assegurar a disponibilidade e qualidade da água e saneamento. Um bom ponto de partida é a indústria monitorar rigorosamente os efluentes que libera no meio ambiente e isso engloba o enquadramento desses efluentes. Essa responsabilidade vai além do cumprimento legal, exigindo uma abordagem proativa para minimizar impactos e contribuir para a preservação dos recursos hídricos.
5. Regulamentações e conformidade: um desafio para a indústria
A implementação do PSA no Brasil é respaldada por diversas regulamentações, incluindo:
– Portaria GM/MS Nº 888/2021: Estabelece padrões de potabilidade da água.
– Resolução CONAMA 357/2005: Define critérios para lançamento de efluentes.
– Resolução SS 195/2024: Exige acreditação de laboratórios para controle de qualidade da água.
5 min leituraHoje dou continuidade à série de posts sobre o evento IFS FOCUS DAY 2024, realizado em São Paulo, em 26 de setembro de 2024. Na ocasião, o Prof. Dr. Romeu […]













 Entretanto, o comportamento invasor de pássaros em instalações industriais, residências, shopping centers, hospitais, escolas e diversas edificações é um fenômeno que foi muito além dos portos e terminais de grãos. Especialmente o pombo urbano (Columba livia) e o pardal (Passer domesticus) desenvolveram uma capacidade de adaptação notável, assumindo habilidades de manobras durante o voo e perícia na construção dos ninhos em locais improváveis.
Entretanto, o comportamento invasor de pássaros em instalações industriais, residências, shopping centers, hospitais, escolas e diversas edificações é um fenômeno que foi muito além dos portos e terminais de grãos. Especialmente o pombo urbano (Columba livia) e o pardal (Passer domesticus) desenvolveram uma capacidade de adaptação notável, assumindo habilidades de manobras durante o voo e perícia na construção dos ninhos em locais improváveis. Estamos de mãos atadas?
Estamos de mãos atadas?