As empresas alimentícias no Brasil têm grandes desafios para atender aos requisitos de segurança dos alimentos fabricados, sobretudo aquelas que dependem de processos bactericidas com a finalidade de manter aos consumidores protegidos contra bactérias como o Clostridium botulinum e suas toxinas.
Este post apresenta um desafio para mim, que é poder explicar de uma forma simples e rápida o que significa verdadeiramente uma validação de processo térmico e ajudar na interpretação do que implica esta validação. Não se deve subestimar a validação quando se tratar da produção de alimentos de baixo teor de acidez selados hermeticamente.
O principal objetivo do tratamento térmico de alimentos enlatados é garantir a destruição de todos os organismos vivos capazes de danificar os alimentos ou prejudicar a saúde do consumidor.
Um processo perfeito do ponto de vista culinário pode não ser suficiente para eliminar os organismos que produzem alterações alimentares.
Por isso, é importante conhecer e definir a intensidade ou grau de aquecimento a que os alimentos enlatados podem ser submetidos para atender as necessidades supracitadas, ou seja, é necessário conhecer e definir o tratamento ou processo térmico. Tal conhecimento, juntamente com o da termorresistência de microrganismos contaminantes, a natureza química e física do alimento e a taxa de penetração do calor são chaves para o sucesso de um correto design de processo térmico.
A natureza química do alimento é muito importante, pois permite classificar os alimentos pela acidez do meio:
Um pH menor que 4,5 categoriza os alimentos ácidos ou acidificados.
Um pH menos ácido (acima de 4,5) categoriza os alimentos com baixo teor de acidez.
Os tratamentos térmicos aplicados aos alimentos ácidos são menos agressivos (temperaturas mais baixas) do que os aplicados aos alimentos não ácidos.
Ao estabelecer a intensidade com que os alimentos enlatados devem ser tratados ou processados, é necessário atentar para as chances de sobrevivência térmica dos esporos.
Para calcular o tempo e a temperatura que devem ser aplicados a um determinado alimento para obter esterilidade comercial, sem afetar sua qualidade, é necessário saber:
- O tempo necessário para que os alimentos atinjam a temperatura desejada.
- O tempo que leva para esfriar
Isso deriva no estabelecimento da taxa de penetração de calor.
No entanto, os fatores que determinam a penetração de calor são:
- Natureza e consistência dos alimentos
- Tamanho e forma do recipiente
- Tipo de material de embalagem
A resistência dos microrganismos ao calor é baseada nos esporos do patógeno mais resistente ao calor encontrado nos alimentos e em condições anaeróbicas, que é o Clostridium botulinum.
Outra bactéria que também é considerada é uma formadora de esporos não patogênica, mas sim deteriorante: Bacillus stearothermophilus.
Seu validador também deve considerar aspectos como a curva de morte térmica, que nada mais é do que a velocidade com que as bactérias morrem durante o aquecimento, sendo quase proporcional ao número presente no alimento que está sendo aquecido, que é igual a uma Ordem Logarítmica de Morte.
Por isso é importante considerar a marcha da morte bacteriana (Ordem Logarítmica de Morte), ao submeter as bactérias ao calor úmido, processo que segue um curso logarítmico. Isso significa que, se uma amostra de um determinado tamanho é aquecida a uma temperatura constante, a mesma proporção de bactérias sobreviventes é destruída em cada unidade de tempo sucessiva.
Em outras palavras, se uma determinada temperatura matar 90% da população de bactérias durante o primeiro minuto de aquecimento, 90% da população restante será morta no segundo minuto, 90% da população restante será morta no terceiro minuto e assim por diante.
A curva de sobrevivência térmica que descreve graficamente o exposto acima pode ser definida pela equação:
T = D (log a-log b)
Onde
T = tempo de aquecimento, em minutos, a uma temperatura constante.
O valor D é o tempo de redução decimal, ou seja, o tempo em minutos a uma temperatura específica necessária para destruir 90% dos organismos em uma população.
O valor “D” diminui a população sobrevivente pelo equivalente a um ciclo logarítmico.
a = número inicial de bactérias viáveis na amostra
b= número de bactérias sobreviventes na amostra.
O valor Z é o número em graus necessário para que uma curva de tempo de morte por calor específico passe por um ciclo logarítmico.
O significado do valor Z caracteriza a resistência das populações bacterianas às mudanças de temperatura.
O valor F é o número de minutos a uma temperatura específica necessária para destruir um número específico de organismos com um valor Z específico. Em outras palavras, é uma medida da capacidade de esterilização de um tratamento térmico.
O valor F de referência F0 é o número em minutos a 121°C necessário para matar um número específico de organismos cujo valor Z é 10°C. Ele é igual ao valor de esterilização.
A fórmula acima pode ser aplicada a uma amostra de qualquer tamanho, desde que os volumes em que (a) e (b) estão contidos sejam iguais. Se a amostra for considerada composta de muitos volumes ou recipientes, à medida que seu número aumenta, o mesmo acontece com o valor de (a) e com o valor de (b). Portanto, em uma série infinita de recipientes ou volumes sempre haverá um contendo uma bactéria sobrevivente, desde que a amostra seja grande o suficiente.
Por exemplo, se um recipiente contém um esporo de Clostridium botulinum com valor D250 de 0,21 minutos e é submetido a um tratamento combinado de tempo e temperatura igual a 2,52 minutos a 250°F, aplicando a equação acima temos que:
2,52 = 0,21 (log1 – log2)
E resolvendo a igualdade,
Log b= -12;
Onde b=10-12.
Isso expressa a probabilidade de que um esporo de C. botulinum sobreviva nesse caso em particular, ou seja, uma chance em 1012.
Como os esporos mais resistentes de C. botulinum têm um valor D de aproximadamente 0,21 minutos a 250°F, eles são submetidos a um processo térmico de 252 minutos 12D a 250°F (assumindo, é claro, que o aquecimento e o resfriamento são instantâneos).
Os pesquisadores Bigelow y Esty e Bigelow, em 1921, foram os primeiros a usar o termo taxa de morte térmica para relacionar a dependência da temperatura de D, de acordo com a seguinte imagem de referência:
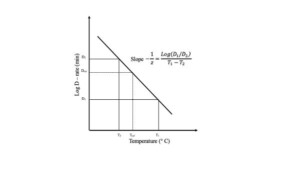
Imagem 1. Curva de tempo de morte térmica (TDT). Fonte: Springer
Valores 12D para outras temperaturas são conhecidos se os logaritmos de tais tempos forem plotados em relação à temperatura correspondente. A curva normal de morte térmica (TDT) é obtida pela inclinação ou declividade da curva designada z, que é numericamente igual ao número de graus Fahrenheit para a curva T.D.T. passar por um ciclo logarítmico. Este valor depende do meio em que a resistência ao calor é estimada, que para esporos de C. botulinum é geralmente tomada como 18°F.
O que significa a letalidade do processo?
Ela representa a soma dos efeitos letais das mudanças de temperatura ao longo do tempo durante todo o funcionamento da autoclave.
A Unidade de Letalidade para cálculos de processo térmico é definida como o calor de remoção equivalente a UM minuto a 121°C contra um organismo com um determinado valor z. Além disso, todas as frações de UM minuto a 121°C ou seus equivalentes representam frações correspondentes de uma unidade de letalidade. Essas frações são conhecidas como “velocidades letais”.
No procedimento para determinação do tempo de processamento e letalidade do processo, as velocidades letais correspondentes às temperaturas sucessivas tomadas das curvas de penetração de calor e resfriamento do processo de autoclave são consideradas e integradas para determinar a letalidade do processo ou seu valor de esterilização (F0).
As velocidades letais são plotadas em função do tempo correspondente às curvas de aquecimento e resfriamento, respectivamente. A área total resultante sob esta curva de taxa letal dividida pela área correspondente a uma unidade de letalidade dá o letal total ou F0.
Importante: este artigo tem como objetivo orientar a indústria de alimentos sobre como interpretar um processo de validação. Ele não consiste em uma metodologia ou procedimento que você deve seguir. Para validação de processo térmico, sugerimos entrar em contato com seu provedor de validação de maior confiança.
Referência bibliográfica
5 min leituraAs empresas alimentícias no Brasil têm grandes desafios para atender aos requisitos de segurança dos alimentos fabricados, sobretudo aquelas que dependem de processos bactericidas com a finalidade de manter aos […]







 Nossas equipes técnicas podem realizar uma análise aprofundada de suas necessidades de testes analíticos, necessidades logísticas e de gerenciamento de dados e procedimentos de amostragem para melhorar seus programas de gerenciamento de segurança. Podemos ajudar os fabricantes de alimentos a implementar ou aprimorar programas de monitoramento ambiental de Listeria e Salmonella e as etapas de controle preventivo de redução de patógenos.
Nossas equipes técnicas podem realizar uma análise aprofundada de suas necessidades de testes analíticos, necessidades logísticas e de gerenciamento de dados e procedimentos de amostragem para melhorar seus programas de gerenciamento de segurança. Podemos ajudar os fabricantes de alimentos a implementar ou aprimorar programas de monitoramento ambiental de Listeria e Salmonella e as etapas de controle preventivo de redução de patógenos. Inajara Juliano é Coordenadora de Expert Services da Mérieux NutriSciences, graduada em Engenharia de Alimentos pela Universidade de Caxias de Sul, com MBA em Engenharia da Qualidade pela POLI-USP. Possui mais de 12 anos de experiência em laboratório, incluindo análises químicas, microbiológicas e gestão da qualidade.
Inajara Juliano é Coordenadora de Expert Services da Mérieux NutriSciences, graduada em Engenharia de Alimentos pela Universidade de Caxias de Sul, com MBA em Engenharia da Qualidade pela POLI-USP. Possui mais de 12 anos de experiência em laboratório, incluindo análises químicas, microbiológicas e gestão da qualidade.
