7 min leituraO que é Sashimi? É um alimento típico da gastronomia e da cultura japonesa feito a partir de pescado cru finamente cortado e acompanhado de molhos diversos, como shoyu ou wasabi. Há alguns anos, o sashimi começou a se expandir pela Europa e América, incluindo a América Latina. Ele apresenta, entre outros perigos biológicos, o parasita Anisakis, de que tratarei neste artigo.
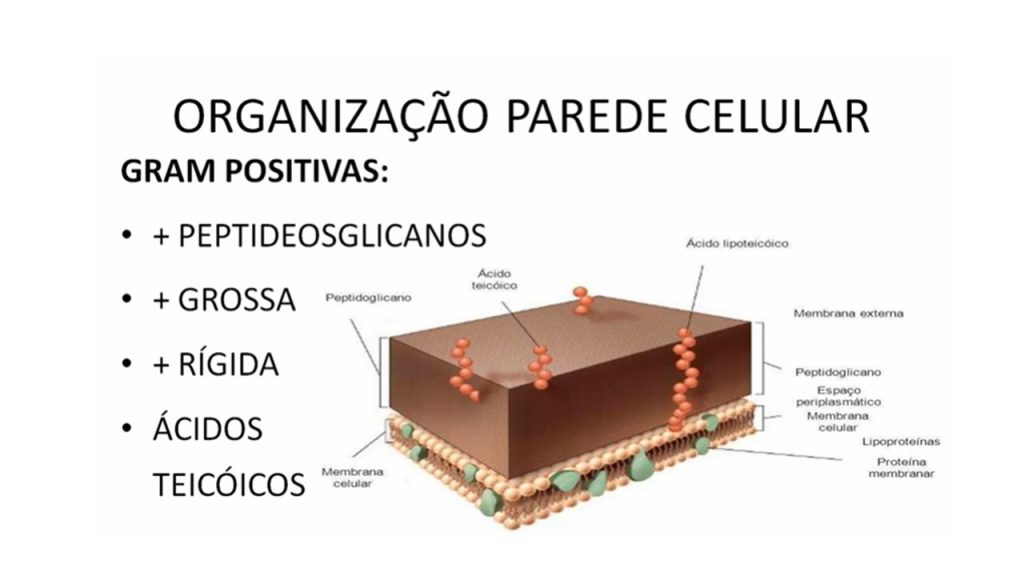
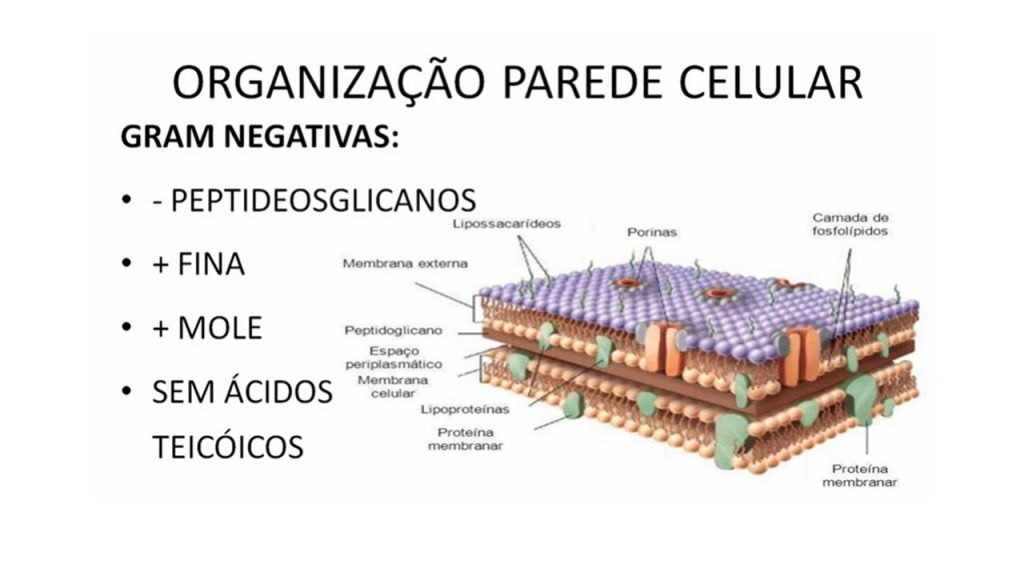
Características gerais dos Anisakis: São nematoides parasitas, em forma de verme, dos quais já foram descritas mais de 25.000 espécies, algumas delas que afetam humanos e outros animais. O mais estudado em relação à ingestão de pescado cru é o Anisakis simplex, frequentemente relacionado ao Sashimi e encontrado em peixes do Oceano Atlântico Sul, como a pescada argentina (Merluccius hubbsi) e outras espécies procedentes de diferentes partes do mundo, com as quais se prepara a especialidade gastronômica japonesa, principalmente atum, salmão, bonito, bacalhau, arenque, anchova e lula.
Na fase adulta, esse parasita vive e se desenvolve no trato gastrointestinal de mamíferos aquáticos, como cetáceos, leões marinhos, golfinhos e focas. Através das fezes dos portadores infestados, os ovos do parasita se disseminam na água, onde cumprem parte de sua evolução até atingir a fase larval (L3) e eclodir. As larvas liberadas na água entram na cadeia alimentar através de pequenos crustáceos e peixes menores, até serem ingeridas por peixes comercialmente importantes, e parasitam principalmente na parede do estômago e intestino, embora também sejam observadas no fígado e nas gônadas.
Como o Anisakis infesta os humanos? Ao comer pescado contaminado que contém as larvas vivas ou viáveis do parasita. Quando o pescado é comido cru ou mal passado, as larvas retêm a capacidade de infestar o homem, atacando o estômago ou a mucosa intestinal, e inclusive enquistando-se nela, causando a doença conhecida como anisaquíase. Os sintomas dessa zoonose podem ser observados em até oito horas após a ingestão das larvas e são caracterizados por cólicas, náuseas, vômitos e diarreia. No caso de afecções intestinais, os sintomas podem demorar até 5 dias a aparecer e podem causar diarreia com sangue. O diagnóstico médico do paciente em geral está relacionado ao consumo de pescado cru ou malpassado e por meio de endoscopia gástrica ou entérica. Por meio da mesma endoscopia, as larvas podem ser removidas e em casos mais graves a cirurgia pode ser necessária. A transmissão ocorre apenas de pescado contaminado para humanos; não é transmitido entre pessoas. No sistema digestivo humano, a larva não pode se desenvolver, pois é um hospedeiro acidental, portanto as fezes humanas não contêm ovos do parasita.
Outro aspecto que pode ser observado acompanhando a infestação de anisakis ou independentemente dela, é a presença de sinais de alergia ao parasita, caracterizados por coceira, vermelhidão da pele e até desconforto respiratório. Em relação à capacidade de induzir uma resposta imune do parasita, ainda há debate entre os pesquisadores: alguns consideram que apenas as larvas vivas ou viáveis ou partes delas são capazes de causar alergia, enquanto outros pesquisadores consideram que mesmo as larvas mortas são capazes de causar sintomas alérgicos em indivíduos suscetíveis, dada a termoestabilidade do antígeno.
Como evitar a anisaquíase?
1- A primeira medida é evitar a pesca nos pesqueiros onde um alto nível de parasitas dos peixes foi confirmado de forma confiável.
2- Como vimos anteriormente, a presença das larvas encontra-se principalmente nas vísceras dos pescados, por isso uma das maneiras mais eficazes de evitar ou diminuir o risco é a evisceração e lavagem da cavidade abdominal com água do mar limpa e seu posterior resfriamento a bordo da embarcação pesqueira ou a evisceração do pescado e lavar a cavidade abdominal o mais rápido possível no estabelecimento de processamento em terra. Os planos de Boas Práticas de Fabricação (BPF) devem levar em consideração esse aspecto, bem como a APPCC e planos de prevenção.
3- Os filés de pescado sem pele devem ser colocados em placas translúcidas, iluminadas por baixo, para verificar a presença de parasitas, por pessoal treinado. A legislação brasileira (Decreto nº 9.013, de 29 de março de 2017, artigo 209 inciso V) indica que “nos estabelecimentos de beneficiamento é obrigatória a verificação visual da presença de parasitas e esse monitoramento deve ser feito por pessoal treinado do estabelecimento”. Caso seja observada a presença do parasita, deve-se retirá-lo com a ponta da faca ou cortar o pedaço de filé parasitado e descartá-lo. Em geral, o Anisakis pode ser encontrado nos músculos da parede abdominal, mas pode eventualmente migrar para outra área. A Norma para filés de peixe ultracongelados do Codex stan 190/1995 diz que “é considerada defeituosa uma amostra que revela a presença de 2 ou mais parasitas por Kg de amostra, encapsulados com mais de 3 mm de diâmetro ou a presença de 1 parasita não encapsulado com mais de 10 mm de comprimento. ”
4- Tratamento térmico. Cozinhar com calor superior a 60°C por pelo menos 2 minutos em todo o peixe inativa o parasita, destruindo sua cutícula protetora. Portanto, ferver pescado (90°C) ou fritar (170°C) são procedimentos altamente eficazes de prevenção. Da mesma forma, congelamento rápido de pescado a -20°C ou mais frio por pelo menos 48 horas, ou congelamento mais lento a -20°C por 7 dias também é eficaz para destruição do parasita.
5- Informações ao consumidor. Em locais onde a doença é pouco conhecida, como países da América Latina, a informação ao consumidor é de vital importância, a fim de prevenir a infestação do Anisakis. Um consumidor informado tem menos probabilidade de sofrer desta doença e, ao consumir pescado cru, deve exigir que ele tenha sido previamente congelado para inativar o parasita.
Como tratar o pescado para que seja seguro comê-lo cru? Nas preparações de pescado cru, como o sashimi e outras especialidades japonesas, a forma de evitar a infestação pelo parasita Anisakis é congelar previamente o pescado ou filé nas condições indicadas no ponto 4.
Peligros del Sashimi: Parásito Anisakis
¿Qué es el Sashimi? Se trata de una comida típica de la gastronomía y de la cultura japonesa hecha a base de pescado crudo finamente cortado y acompañado por diferentes salsas, como ser de soja o wasabi, que desde hace algunos años comenzó a expandirse por Europa y América, incluyendo Latinoamérica y que presenta, entre otros peligros biológicos, al parásito Anisakis, del cual me voy a ocupar en este artículo.
Características generales de Anisakis: Se trata de vermes nematodos, con forma de gusano, del cual se han descrito más de 25.000 especies, siendo algunas de ellas parásitos que afectan al ser humano y otros animales. El más estudiado en relación a la ingestión de pescado crudo es el Anisakis simplex, al que de forma frecuente se relaciona con el Sashimi y que se encuentra en peces del Océano Atlántico sur, como ser la merluza argentina (Merluccius hubbsi) y de otras especies de diversas partes del mundo, con las que se prepara la especialidad gastronómica japonesa, principalmente atún, salmón, bonito, bacalao, arenque, anchoa y calamar.
En su etapa adulta, este parásito vive y se desarrolla en el tracto gastrointestinal de los mamíferos acuáticos, como ser los cetáceos, lobos marinos, delfines y focas. A través de las heces de los portadores infestados, se diseminan los huevos del parásito en el agua, donde cumplen parte de su evolución hasta convertirse en el estado larvario (L3) y eclosionan. Las larvas liberadas al agua ingresan en la cadena alimentaria por medio de pequeños crustáceos y peces de menor tamaño, hasta llegar a ser ingeridos por los peces de importancia comercial, a los cuales parasitan principalmente en la pared del estómago e intestino, aunque también se les ha observado en el hígado y gónadas.
¿Cómo llega el Anisakis a infestar al ser humano? Comiendo pescado que contenga la larva viva o viable del parásito. Cuando el pescado se consume crudo o insuficientemente cocido, la larva conserva su capacidad de infestar al ser humano, atacando la mucosa estomacal o la mucosa intestinal e incluso enquistándose en ella, provocando la enfermedad conocida como anisakiasis. Los síntomas de esta zoonosis, se pueden observar dentro de las ocho horas luego de ocurrida la ingestión de la larva y se caracterizan por cólicos, nauseas, vómitos y diarrea. En el caso de afección intestinal, los síntomas pueden tardar hasta 5 días en manifestarse y puede causar diarrea sanguinolenta. El diagnóstico médico del paciente en general se relaciona con el consumo de pescado crudo o insuficientemente cocido y por medio de endoscopía gástrica o entero-gástrica. Por medio de la misma endoscopía se puede retirar la/las larvas y en casos más graves puede ser necesaria la cirugía. La contaminación solo se produce desde el pescado contaminado al ser humano; pero no se transmite entre personas. En el aparato digestivo humano la larva no puede desarrollarse, por tratarse de un hospedador accidental, por lo que las heces humanas no contienen huevos del parásito.
Otro aspecto que puede observarse acompañando a la infestación por anisakis o independientemente de ella, es la aparición de signos de alergia al parásito, caracterizados por prurito, enrojecimiento de la piel, picor e incluso puede observarse dificultad respiratoria. Con respecto a la capacidad de alergenicidad del parásito, hay todavía discusión entre los investigadores; algunos consideran que solamente la larva viva o viable o partes de ella, es capaz de causar alergia, mientras otros investigadores consideran que aún la larva muerta es capaz de causar síntomas de alergia en individuos susceptibles, dada la termoestabilidad del antígeno.
¿Cómo evitar la anisakiasis?
- La primera medida, es evitar pescar en los caladeros donde se ha confirmado fehacientemente un alto tenor de parasitación de los pescados.
- Como hemos visto anteriormente, la presencia de las larvas se encuentra principalmente en las vísceras del pescado, por lo que la evisceración y el lavado de la cavidad abdominal con agua de mar limpia y su posterior enfriado a bordo del buque pesquero o, la evisceración del pescado y el lavado de la cavidad abdominal lo antes posible en el establecimiento de procesado en tierra firme, es una de las formas más eficaces de evitar o disminuir el peligro. Los planes de Buenas Prácticas de Manufactura (BPM), deben tener en cuenta este aspecto, así como en el Análisis de Peligros Biológicos y su prevención.
- Los filetes de pescado sin piel deben ser colocados en placas traslúcidas, iluminadas desde abajo para buscar la presencia de parásitos, por personal capacitado. La legislación de Brasil (Decreto n° 9013, de 29 de marzo de 2017 artículo 209 punto V), indica que “en los establecimientos de pescado es obligatoria la verificación visual de la presencia de parásitos y este monitoreo debe ser realizado por personal capacitado del establecimiento”. En caso de observarse la presencia de parásito se deberá quitar con la punta del cuchillo o cortar el trozo de filete parasitado y desecharlo. En general al Anisakis se le puede encontrar en la musculatura de la pared abdominal, pero puede migrar hacia otra zona. En la Norma para filetes de pescado congelados rápidamente del Codex stan 190/1995, “Es considerada defectuosa una muestra que revele la presencia de 2 o más parásitos por Kg de muestra, encapsulado con más de 3 mm de diámetro o la presencia de 1 parásito no encapsulado con más de 10 mm de largo.”
- Tratamiento térmico. La cocción por calor que supere los 60°C por al menos 2 minutos en toda la pieza del pescado, inactiva al parásito por destrucción de su cutícula protectora. Por lo tanto hervir el pescado (90°C) o la fritura (170°C), son procedimientos de alta eficacia para la prevención. Asimismo la congelación rápida del pescado a -20°C o más frío por al menos 48 horas, o una congelación más lenta que alcance los -20°C durante 7 días, también es efectiva para la destrucción del parásito.
- Información al consumidor. En lugares donde esta enfermedad es poco conocida, como son los países latinoamericanos, la información al consumidor es de vital importancia, a los efectos de prevenir la infestación por Anisakis. Un consumidor informado está menos propenso a padecer esta enfermedad y cuando consuma pescado crudo debe exigir que previamente haya sido congelado de forma de inactivar el parásito.
¿Cómo tratar el pescado para que sea seguro su consumo crudo? En las preparaciones de pescado crudo, como el Sashimi y otras especialidades japonesas, la forma de evitar la infestación con parásito Anisakis, es congelar previamente el pescado o el filete en las condiciones indicadas en el numeral 4.
Fontes / Fuentes consultadas:
http://www.aecosan.msssi.gob.es/AECOSAN/web/seguridad_alimentaria/subdetalle/anisakis.htm https://foodsafetybrazil.org/bpf-em-supermercados-as-instrucoes-de-trabalho-sao-uma-carta-na-manga/http://seafoodbrasil.com.br/novo-memorando-de-parasitas-mapa-preocupa-industria-e-importadores/DECRETO Nº 9.013, DE 29 DE MARÇO DE 2017– (Legislación de Brasil)
https://definicion.de/zoonosis/
Texto em espanhol não revisado por nossa redação
7 min leituraO que é Sashimi? É um alimento típico da gastronomia e da cultura japonesa feito a partir de pescado cru finamente cortado e acompanhado de molhos diversos, como shoyu ou […]