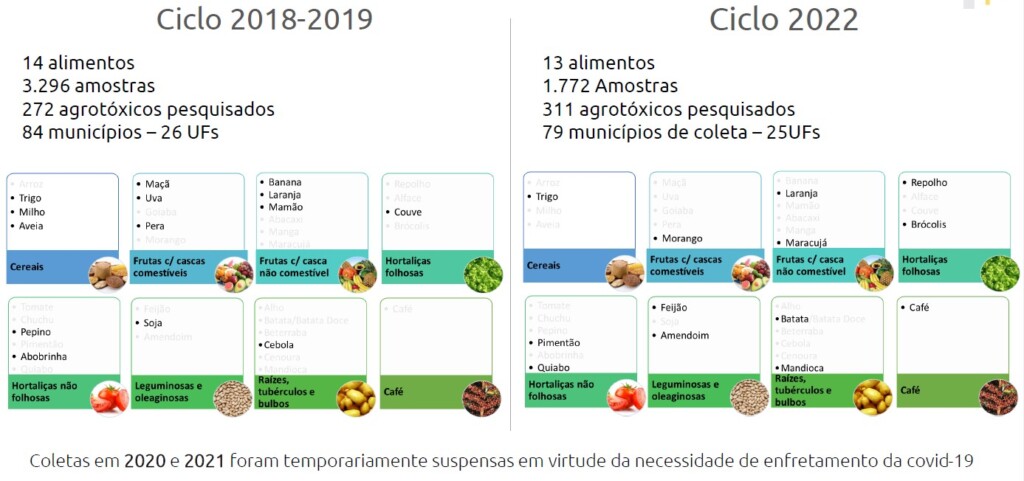
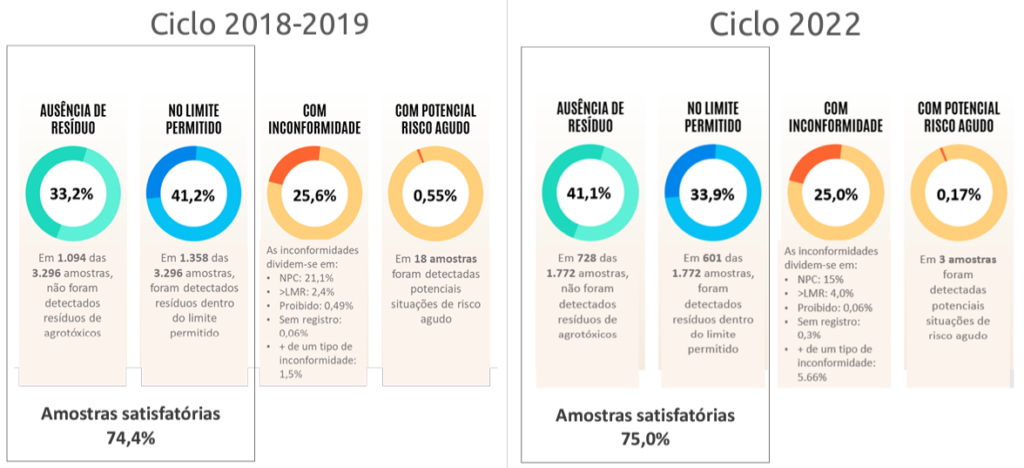
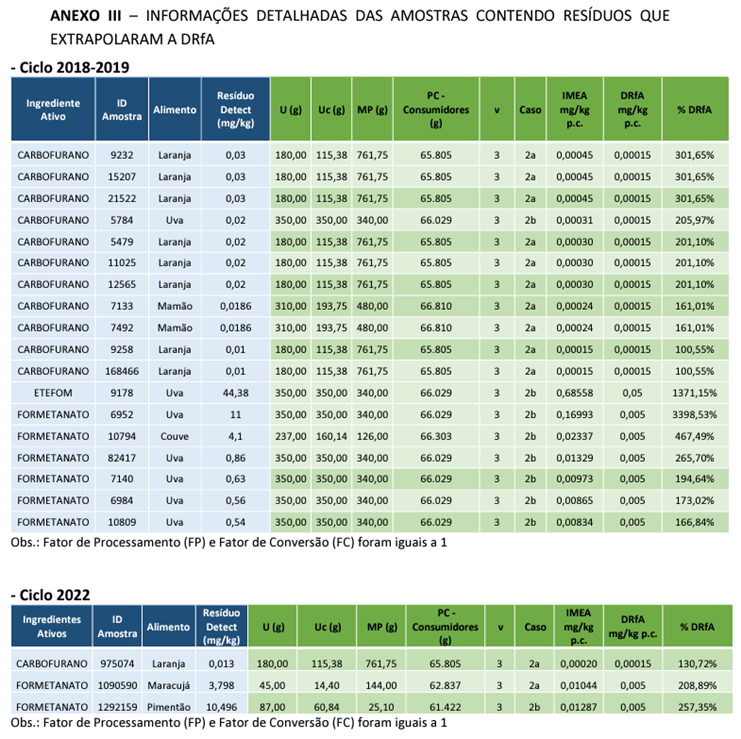
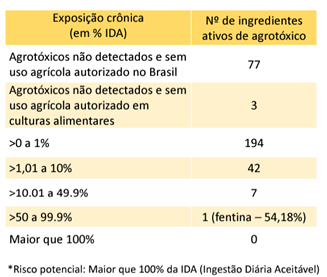
10 min leituraO uso de ozônio vem sendo cada vez mais divulgado na cadeia produtiva de alimentos, demonstrando sua enorme eficácia e diversidade de aplicações neste setor. Veja por exemplo, aqui, o post da palestra de Vivaldo Mason no V Workshop Food Safety Brazil, em junho de 2022, em Goiânia. Entretanto, o ozônio ainda é pouco utilizado para esse tipo de indústria. Uma das razões é que muitos desconhecem COMO MEDIR ozônio na água ou no ar e, por isso, ficam inseguros em avançar na adoção do ozônio. Este post tem o objetivo de preencher essa lacuna no conhecimento de muitos profissionais de indústrias de alimentos do Brasil.
1. Medição da concentração de ozônio na água ozonizada*
A concentração de ozônio na água pode ser medida por meio de duas tecnologias principais: kits de teste colorimétrico ou medidores eletrônicos.
1.1 Métodos colorimétricos para medição de ozônio dissolvido em água
Os métodos colorimétricos são classificados como indiretos porque utilizam reações específicas para medir ozônio e a quantificação é possível a partir do produto da reação ou degradação do reagente específico. Estes métodos são muito utilizados e possuem um custo mais baixo quando comparados ao método direto, principalmente devido à simplicidade instrumental das medidas realizadas.
1.1.1 Método colorimétrico índigo
O método de índigo utiliza o reagente químico índigo trisulfonato que reage instantaneamente e quantitativamente com o ozônio, alterando a tonalidade da cor azul do reagente em proporção direta com a quantidade de ozônio presente. Ácido malônico é adicionado ao reagente e está incluído na ampola para impedir a interferência de até 3ppm de cloro. Os resultados são expressos em ppm (ou mg / L) de O3.
Depois, a solução ozonizada passa a ser analisada por um analisador colorimétrico calibrado que avalia a concentração de ozônio dissolvido. Existem fabricantes que fornecem um kit contendo um reagente químico em ampolas, selado a vácuo e um colorímetro que avalia por meio de lâmpadas e sensores a alteração da tonalidade, obtendo a concentração de ozônio.
Desta forma, os valores obtidos são convertidos em ppm (mg/L) de ozônio dissolvido com a tabela de calibração incluída no equipamento.

Figura 1: Método Índigo para medição de ozônio dissolvido.
Fonte: fabricante
1.1.2 Método DPD
O método utilizado para medir ozônio é o DDPD (uma forma de DPD substituída com metil, que é N, N-dietil-p-fenilenodiamina) desenvolvido e patenteado pela empresa Chemetrics®. A solução ativadora de iodeto de potássio é adicionada à amostra antes da análise. O ozônio reage com o ânion iodeto para liberar iodo livre. O iodo, em seguida, reage com o reagente para produzir um DDPD azul-violeta. Pela intensidade da cor, mede-se a concentração. Vários halógenos livres também podem produzir cor azul-violeta com o reagente DDPD, e, portanto, interferir na análise de ozônio.

Figura 2: Métodos DPD para medição de ozônio dissolvido.
Fonte: fabricante
1.2 Métodos eletrônicos para medir ozônio em água
1.2.1 Monitores eletrônicos
Os monitores ou controladores eletrônicos para medir ozônio dissolvido usam um amperímetro coberto por membrana permeável mantendo-a esticada firmemente sobre um cátodo de ouro ou platina.
Uma solução de ânodo e eletrólito de prata completa o circuito interno. Durante a operação, o ozônio difunde-se da amostra através da membrana. Uma vez dentro do sensor, o ozônio reage com a solução eletrolítica para formar um composto intermediário. Uma tensão de polarização aplicada ao cátodo reduz completamente esse composto intermediário, produzindo uma corrente entre o cátodo e o ânodo medido pelo analisador.
Essa corrente é diretamente proporcional à taxa na qual o ozônio se difunde através da membrana para o sensor, o que é proporcional à concentração de ozônio na solução. As desvantagens são seu custo de aquisição mais alto. Uma vantagem do método eletrônico é que ele mede a amostra em tempo real e permite controlar o gerador de ozônio para manter os níveis de ozônio dissolvidos desejados.

Figura 3: Métodos Eletrônico para medição de ozônio dissolvido.
Fonte: fabricante
1.2.2 Método ORP para medição de ozônio em água
ORP significa “Oxidation Reduction Potential”, em português: Potencial de Redução de Oxidação, que é medido por uma sonda ORP. Em termos práticos, é um voltímetro que mede a tensão (em milivolts) através de um circuito formado por um eletrodo de referência construído com fio de prata (polo negativo) e um eletrodo de medição construído de uma banda de platina (polo positivo) com uma solução eletrolítica no meio.
Embora o ORP não meça o ozônio dissolvido e sim condutividade elétrica (a menos que o ozônio seja única substância oxidante presente na solução), ele pode ser muito útil para controlar a produção de geradores de ozônio em água que não contenha cloro, pois o cloro pode interferir na análise por ORP. Um exemplo deste tipo de medidor é em mineradores de água potável. Quando um nível predefinido de ORP é excedido, um sinal elétrico é enviado ao gerador de ozônio para diminuir a produção de ozônio e vice-versa.
O eletrodo de referência é cercado por uma solução de água e sal (eletrólito), que produz outra pequena tensão. A voltagem produzida pelo eletrodo de referência é constante e estável, portanto, fornece uma referência contra a qual a voltagem gerada pelo eletrodo de medição de platina e pelos oxidantes na água pode ser comparada.
A diferença de tensão entre os dois eletrodos está no que é realmente medido pelo medidor. Nota: pH alto ou baixo pode alterar as leituras de ORP envolvendo ozônio dissolvido devido à rápida decomposição do ozônio em pH elevado. A precisão ideal requer níveis de pH entre 6,5 e 8,0.

Figura 4: Medidor ORP para medição de ozônio
Fonte: fabricante
2. Medição de concentração de gás ozônio no ar
Sabe-se que o ozônio gasoso pode ser perigoso em altas concentrações. As empresas devem garantir que em locais habitados sejam usadas doses seguras, e nas áreas inabitadas não deve haver vazamentos para ambientes habitados. Para isso, a área deve ser monitorada para segurança das pessoas e para garantir que as concentrações apropriadas de ozônio estejam disponíveis para os fins a que se destinam.
O ozônio na fase gasosa pode ser uma ferramenta muito benéfica na indústria de processamento de alimentos. O armazenamento de alimentos processados em atmosferas modificadas contendo pequenas quantidades de ozônio gasoso ajuda no controle de bolores, leveduras e muitos contaminantes transportados pelo ar, tanto nos produtos alimentícios quanto nas superfícies das prateleiras de armazenamento e outros equipamentos.
Os ambientes com “atmosfera modificada” rica em ozônio representam as aplicações eficientes para redução de microrganismos em alimentos, mas também existem outros usos, principalmente para controle de pragas em produtos agrícolas armazenados, maturação para amaciamento de carne, armazenamento de barris de vinhos, cura de queijos etc.
Dentre as tecnologias para medir ozônio gasoso, temos:
1) adsorção de UV,
2) tecnologia de semicondutor de óxido metálico e
3) método iodométrico.
2.1 Medição de ozônio através de adsorção de radiação UV
A técnica de adsorção da radiação na região do ultravioleta é utilizada como um método direto de determinação, pois é medida diretamente a adsorção do ozônio. Esse método tem como característica a resposta próxima ao tempo real e a técnica possui sensibilidade muito precisa.
Os medidores que utilizam a tecnologia de UV são amplamente utilizados para determinar níveis de ozônio tão baixos quanto as quantidades atmosféricas típicas (menor de 0,10 ppm) até concentrações elevadas produzidas por verdadeiras usinas de ozônio com produção de 50kg a 250 kg/hora, muito usadas em tratamento de água de cidades operando com concentrações acima de 160-250 mg/L.
O método UV é muito preciso (±1%), a tecnologia é dominada por poucas empresas fabricantes. Seu custo de aquisição é alto e um equipamento custa em média USD 4.800.00 (quatro mil e oitocentos dólares) nos EUA, € 4.000,00 (quatro mil euros) na Europa e USD 2.000.00 (dois mil dólares na China).
As unidades de leituras também podem estar em peso (wt%), ou em volume podendo ser medido em partes por milhão (ppm), partes por bilhão (ppb), gramas por metro cúbico (g/m³), gramas por metro cúbico normalizado (g/Nm³), miligramas por metro cúbico (mg/m³) e miligramas por litro (mg/L).
O ozônio gasoso entra no analisador de ozônio por meio de mangueiras, preenchendo uma câmara interna que possui um sensor em uma extremidade e uma lâmpada UV do outro lado da câmara. Ao inserir o gás ele vai reagir com a radiação UV emitida pela lâmpada e o sensor fornecerá a leitura de acordo com a concentração de ozônio analisada. Quanto maior a concentração, menor será a leitura pelo sensor de UV.
Além de analisarem a concentração de ozônio, estes equipamentos também podem analisar outros dados como pressão atmosférica e temperatura do gás. Os equipamentos mais completos possuem “data logger” (capacidade de armazenar informações na memória do equipamento) e depois pode-se extraí-los por meio de uma “porta serial” ou “porta USB” para computadores por meio de um software que permite a emissão de relatórios.
Alguns fabricantes estão desenvolvendo modelos mais simples e com menos recursos, o que reduzirá o preço destes equipamentos e facilitará o acesso das empresas.

Figura 5: Diagrama esquema montagem do analisador de ozônio por absorção UV.
2.2 Medição de ozônio através de semicondutores de óxido metálico (MOS)
Esta tecnologia chama-se “Metal Oxide Semiconductor (MOS)”, em português: semicondutores de óxido metálico. Estes analisadores de ozônio em fase gasosa baseados na tecnologia MOS são mais baratos que os analisadores de UV (média de USD 100 nos EUA) e são normalmente usados em situações em que é necessário medir ozônio em concentrações baixas e com precisão menos exigente, pois sua leitura é aproximada. A faixa de leitura varia de 0 a 100ppm. O sensor necessita ser trocado periodicamente (média de 6 meses) de acordo com o tempo de utilização para garantir leitura mais precisa.
O sensor modelo MQ131 foi desenvolvido pela Hanwei Eletronics e baseia-se em uma pastilha semicondutora que ao ser montada em um circuito nas especificações do fabricante, emite uma ionização que atrai moléculas de ozônio presentes na atmosfera para o sensor. Quando o ozônio entra em contato com a superfície do sensor, libera elétrons. O sensor transforma estes elétrons em corrente elétrica medidos em milivolts. A leitura varia de acordo com a variação da concentração de ozônio em que o equipamento foi instalado.

Figura 6: Sensor pastilha semicondutora
Os sensores MOS são amplamente utilizados como dispositivos de segurança de parede ou portáteis conhecidos por detectores de ozônio para avisar os operadores se os níveis de ozônio excedem uma concentração segura. Quando isto acontece, emitem um sinal sonoro e/ou luminoso. As unidades MOS estão disponíveis nos formatos de fixação na parede, manual e até pessoal podendo ser carregado no cinto do operador. Os sensores precisam ser substituídos a cada 6 a 12 meses, dependendo do período e concentração em que ficaram expostos.

Figura 7: Unidades MOS (parede, manual)
2.3 Método Iodométrico para quantificação de ozônio gasoso
O método iodométrico, também conhecido como método por iodeto de potássio ou método KI, é um procedimento padronizado usado para medir ozônio gasoso. Este método é reconhecido e usado por fabricantes de geradores de ozônio de todo mundo na calibração de seus equipamentos. O procedimento oficial foi estabelecido por membros do Comitê de Garantia de Qualidade da International Ozone Association (IOA)**, incluindo a Pan-Americana Group (PAG), European African Group (EAG) e Nippon Islands Group (NIG).
A iodometria é um método volumétrico indireto onde um excesso de íons iodeto é adicionado a uma solução contendo o agente oxidante que irá reagir produzindo iodo que será titulado com solução padronizada de tiossulfato de sódio (Na2S2O3). Por esta razão, o método iodométrico é considerado um método de quantificação de ozônio indireto. Na determinação da concentração de ozônio gasoso, o agente oxidante é o próprio gás que é incorporado a solução de iodeto de potássio KI (2%) através de borbulhamento.
Os íons iodetos (I-) em contato com ozônio são reduzidos a iodo (I2) de acordo com a reação apresentada abaixo. A reação de formação do iodo em meio neutro é lenta, mas sua velocidade aumenta com a diminuição do pH, que é alcançado com a adição de solução de ácido sulfúrico 1N.
O3 + 2KI + H2O I2 + O2 + 2KOH
O iodo presente em uma solução aquosa de iodeto tem uma cor intensa amarelo-castanha. Quando se titulam soluções incolores com uma solução-padrão de iodo, o próprio iodo serve como indicador. Em iodometria é comum o uso de indicadores auxiliares porque a viragem é menos perceptível, devido ao cansaço visual a que o analista é submetido. O indicador auxiliar geralmente utilizado na quantificação de ozônio é uma solução aquosa de amido, com a qual se pode determinar concentrações de iodo em solução de até 2 x 10-7 mol.L-1.
O amido é uma substância formada por 2 constituintes macromoleculares lineares, chamados amilose (alfa-amilose) e amilopectina (beta-amilose). Estas substâncias formam complexos de adsorção (complexos de transferência de carga) com o iodo. No caso da amilose, que possui conformação helicoidal, acredita-se que a cor azul intensa seja resultante da adsorção do iodo (na forma I5-) nestas cadeias. Já o complexo iodo-amilopectina produz uma cor violácea, de forma irreversível. Desta forma, o amido solúvel comercializado para uso como indicador deve consistir basicamente em amilose, separada da amilopectina.
A solução de amido, se não preservada convenientemente (em local refrigerado a 5ºC), decompõe-se em poucos dias, principalmente por causa de ações bacterianas e dos produtos de sua decomposição. Isto pode interferir nas propriedades indicadoras do amido.
3. Rastreabilidade da calibração de equipamentos
Existem diversos métodos para medição de ozônio em água e no ar com diferentes custos, praticidade e precisão. No caso de indústrias de alimentos que precisam assegurar a rastreabilidade da calibração de seus instrumentos para medir ozônio, como por exemplo indústrias certificadas ISO 22000, FSSC 22000, BRC Food ou IFS Food, os equipamentos devem ser calibrados utilizando métodos oficiais reconhecidos.
No caso da medição do ozônio em água, o método reconhecido é o Método Colorimétrico Índigo, mencionado no ítem 1.1.1 e detalhado no Standard Methods** sob o código 4500-O3 OZONE (RESIDUAL) que foi aprovado pelo Standard Methods Committee, 1997 e revisado em 2011.
No caso de medição de ozônio no ar ou na saída do gerador, o método de referência é o método iodométrico referenciado no Standard Methods sob o número 2350 D, que também é citado pela IOA – International Ozone Association***, mencionado no item 2.3 deste artigo.
Referências
*. Filho, Vivaldo M., Ozônio na Indústria de Alimentos, Editora Garcia, 287 páginas.
**. Standard Methods for Water and Waste Water, 24ª Edição. Ver em www.standardmethods.org
***. IOA – International Ozone Association. https://www.tandfonline.com/doi/abs/10.1080/01919519608547327
10 min leituraO uso de ozônio vem sendo cada vez mais divulgado na cadeia produtiva de alimentos, demonstrando sua enorme eficácia e diversidade de aplicações neste setor. Veja por exemplo, aqui, o […]