Conteúdos
Segundo dados da ABIAD (Associação Brasileira da Indústria de Alimentos para Fins Especiais e Congêneres), o consumo de suplementos alimentares no Brasil cresceu cerca de 10% nos últimos cinco anos, impulsionado especialmente pela pandemia, que reforçou a importância da imunidade e da saúde preventiva. As projeções indicam um crescimento anual composto (CAGR) de aproximadamente 6,4% entre 2025 e 2030, configurando um cenário favorável tanto para empresas consolidadas quanto para novos fabricantes, estimulando a inovação e o desenvolvimento de formulações voltadas a um público cada vez mais atento à manutenção da saúde e bem-estar.
Com esse crescimento, intensifica-se a necessidade de regulamentações e controles rigorosos que assegurem a qualidade, segurança e eficácia dos suplementos alimentares ao longo de toda sua vida útil. De acordo com o art. 10 da RDC nº 243/2018, a manutenção das características dos suplementos até o final do prazo de validade deve ser garantida pelo fabricante, considerando as condições de armazenamento e preparo indicadas. O § 1º do mesmo artigo estabelece que essa garantia deve estar respaldada por estudos de estabilidade e controles de qualidade adequados.
O que é estabilidade em suplementos alimentares?
A estabilidade, ou prazo de validade, corresponde ao intervalo de tempo durante o qual o produto permanece seguro e adequado para consumo, desde que mantido nas condições de armazenamento especificadas pelo fabricante. Na prática, isso implica que o suplemento deve:
- Permanecer isento de riscos microbiológicos, não causando infecções ou intoxicações alimentares;
- Manter suas características nutricionais conforme declaradas na tabela nutricional, sem degradação significativa de macro e micronutrientes;
- Preservar atributos sensoriais e físico-químicos, garantindo a aceitação e eficácia até o final do prazo de validade.
Nos suplementos alimentares, o estudo de estabilidade assume papel ainda mais crítico, uma vez que se deve comprovar não apenas a ausência de alterações sensoriais ou deterioração, mas também a manutenção quantitativa dos nutrientes declarados, como vitaminas e minerais. Um exemplo prático: ao adquirir um suplemento de vitamina C próximo à data de vencimento, a concentração declarada ainda é a mesma? A resposta somente pode ser obtida por meio de dados provenientes de estudos de estabilidade conduzidos de forma científica e documentada.
Fatores que influenciam a estabilidade
Diversos fatores interferem na estabilidade dos suplementos alimentares, incluindo:
- Temperatura e umidade;
- Exposição ao oxigênio e à luz;
- pH da formulação;
- Presença de agentes oxidantes ou redutores, íons metálicos e outros ingredientes;
- Tipo e desempenho da embalagem, que exerce papel fundamental na proteção contra degradação físico-química.
Essas variáveis devem ser cuidadosamente avaliadas no planejamento e condução dos estudos de estabilidade, pois pequenas variações podem impactar significativamente o desempenho e a eficácia do produto.
Guia da Anvisa e metodologias aplicáveis
Em abril de 2025, a Anvisa publicou a terceira versão do “Guia n°16 para Determinação de Prazos de Validade de Alimentos”, que fornece recomendações técnicas e exemplos práticos sobre os aspectos a serem considerados na definição do prazo de validade. O documento descreve diferentes abordagens metodológicas, divididas em duas principais categorias:
- Métodos diretos: envolvem o monitoramento da qualidade do produto sob condições controladas de armazenamento, por um período equivalente ou superior ao prazo de validade proposto. Esse método permite observar alterações reais no produto, fornecendo dados robustos para estimar a validade.
- Métodos indiretos (acelerados): utilizam condições ambientais mais severas, como temperaturas elevadas, para acelerar reações de degradação, permitindo previsões em menor tempo. Embora mais rápidos, esses métodos exigem compreensão detalhada dos mecanismos de deterioração e extrapolação cuidadosa dos resultados para condições normais.
Estudos de estabilidade acelerados e de longa duração
Os estudos acelerados são conduzidos sob condições controladas de 40°C ± 2°C e 75% ± 5% de umidade relativa (UR), permitindo prever o comportamento do produto em menor tempo. Embora úteis para uma avaliação preliminar, esses estudos não substituem os ensaios de longa duração, realizados sob condições que simulam a zona climática IVb (30°C ± 2°C e 75% ± 5% UR), representativa do ambiente brasileiro. Os estudos de longa duração são essenciais para comprovar a estabilidade real do produto ao longo do tempo, garantindo que os suplementos mantenham suas propriedades até o fim da validade.
Documentação e requisitos regulatórios
Os relatórios de estabilidade devem ser elaborados de forma técnica, detalhada e rastreável, conforme o disposto no Anexo X da Instrução Normativa nº 281, de 22 de fevereiro de 2024, que define a documentação exigida para regularização de alimentos e embalagens conforme a categoria de produto.
Esse relatório deve conter:
- Descrição das condições de armazenamento, tempos e ensaios realizados;
- Resultados dos ensaios dos parâmetros físico-químicos, microbiológicos e sensoriais;
- Gráficos e tabelas que evidenciam tendências e variações ao longo do tempo;
- Laudos analíticos anexados, com metodologias validadas, precisas e exatas, assegurando a confiabilidade dos resultados.
A robustez dos estudos de estabilidade é determinante para a credibilidade técnica do fabricante e para a conformidade regulatória, além de garantir ao consumidor um produto seguro, eficaz e de qualidade até o último dia de validade.
Desafios e tendências na avaliação de estabilidade
A condução de estudos de estabilidade em suplementos alimentares apresenta desafios específicos, especialmente devido à complexidade das formulações e à presença de nutrientes sensíveis, como vitaminas hidrossolúveis, ácidos graxos poli-insaturados e probióticos. Entre as tendências observadas, destacam-se:
- Uso de tecnologias de proteção, como microencapsulação, spray drying e lipossomas, que aumentam a estabilidade e biodisponibilidade de compostos ativos;
- Adoção de embalagens ativas, que liberam ou absorvem substâncias com o objetivo de manter ou melhorar as propriedades sensoriais, microbiológicas e químicas do alimento durante o armazenamento;
- Integração de ferramentas preditivas e modelagem cinética, que permitem prever o comportamento de degradação sem depender exclusivamente de testes de longa duração;
- Aprimoramento de métodos analíticos com maior sensibilidade e precisão, alinhados a guias de validação internacionalmente aceitos (como AOAC e ISO).
Essas estratégias fortalecem o controle da estabilidade e contribuem para otimizar o ciclo de desenvolvimento e registro de produtos, mantendo o compromisso com a qualidade e a transparência ao consumidor.
Em síntese, o estudo de estabilidade é um pilar essencial para o desenvolvimento, registro e manutenção da qualidade dos suplementos alimentares. Ele garante que os produtos mantenham sua eficácia e segurança durante todo o prazo de validade declarado, refletindo o compromisso das empresas com as boas práticas de fabricação e a conformidade regulatória. Com o avanço das metodologias analíticas e o aprimoramento das diretrizes regulatórias, o setor de suplementos tem à disposição ferramentas cada vez mais precisas para demonstrar a consistência e a integridade de seus produtos, fortalecendo a confiança do consumidor e promovendo a sustentabilidade do mercado.
Lilian Carezia é consultora do Instituto SENAI de Tecnologia em Alimentos e Bebidas, Chapecó/SC.
4 min leituraSegundo dados da ABIAD (Associação Brasileira da Indústria de Alimentos para Fins Especiais e Congêneres), o consumo de suplementos alimentares no Brasil cresceu cerca de 10% nos últimos cinco anos, […]
Chegamos ao último post que nos coloca a par do maior surto de botulismo já registrado na história – apesar de ocorrer nos Estados Unidos, lembre-se de que o produto era comercializado também no Brasil. O que sabemos até o momento? Quais foram os esforços internacionais e qual o impacto deste surto no futuro? Para acessar os outros posts desse assunto, acesse aqui e aqui.
O que se sabe, esforços internacionais e perspectiva de futuro
Como resposta ao surto, a FDA está trabalhando em conjunto com especialistas internacionais e entidades de padronização para avaliar o risco do Clostridium botulinum em fórmulas infantis, enquanto investiga a origem desse surto específico. Além disso, estão analisando os ingredientes lácteos da cadeia de suprimentos e ampliando o conhecimento científico sobre esta bactéria. Já fortaleceram a comunicação com a indústria, consumidores e órgãos de saúde, visando minimizar riscos futuros e garantir a segurança das fórmulas infantis. No entanto, os resultados das investigações até agora não foram conclusivos, e o nome do fornecedor do leite em pó não foi revelado.
É sabido que os esporos de Clostridium botulinum estão presentes em baixos níveis em diversos alimentos, e a presença deles não implica necessariamente em risco, pois nem todos são viáveis para provocar a doença. No entanto, a bactéria é extremamente resistente e consegue sobreviver a pasteurização convencional e a condições ambientais desfavoráveis por longos períodos, graças a um esporo protetor, o que significa que os esporos podem não ser eliminados durante o processamento.
A Agência está empenhada em entender melhor os fatores que levaram a este surto e busca preencher as lacunas no conhecimento científico sobre o Clostridium botulinum. Na 55ª Sessão do Codex Committee on Food Hygiene, sugeriu-se que a JEMRA — reunião conjunta de especialistas da FAO e da OMS — conduza uma avaliação de risco microbiológico voltada a patógenos formadores de esporos, como Clostridium botulinum e Bacillus cereus, em fórmulas infantis em pó. Da mesma forma, foram requeridas outras orientações sobre medidas de controle na fabricação de fórmulas infantis, desde a produção inicial e embalagem até a reconstituição do produto, englobando o monitoramento ambiental. O encontro ocorreu de 15 a 19 de dezembro de 2025, na cidade de Nashville, nos Estados Unidos.
Em resposta, a FAO e a OMS fizeram um apelo internacional, inclusive com abertura de seleção de vagas de especialistas que queiram contribuir com conhecimento científico na avaliação de risco microbiológico destas fórmulas. Os dados servirão como subsídios para o desenvolvimento de pareceres científicos que orientarão a revisão dos documentos atuais do Codex Alimentarius e a elaboração dos textos pertinentes. O esforço é global para entender melhor os riscos de patógenos formadores de esporos. Além disso, busca-se estimar a carga de doenças atribuíveis a esses microrganismos e suas toxinas associadas ao consumo de fórmulas. Também se pretende determinar a prevalência e os níveis de contaminação desses patógenos desde a produção até o momento do consumo. Além disso, solicitaram que governos, indústria, academia, laboratórios e quaisquer outras organizações e indivíduos interessados ??enviem quaisquer dados e informações disponíveis que possam contribuir para este trabalho até 15 de maio. A avaliação dos candidatos será realizada em 15 de março de 2026, até que se tenha um número suficiente de candidatos interessados.
Com o objetivo de estabelecer estratégias para reduzir riscos e garantir a segurança da fórmula infantil em pó no futuro, a FDA lançou a página intitulada “Ações da FDA para Responder a Doenças Causadas por Clostridium botulinum Associadas ao Consumo de Fórmula Infantil em Pó”.
Todas as fórmulas infantis deverão realizar análise para Clostridium?
Os Estados Unidos iniciaram, em fevereiro, testes extensivos dos componentes utilizados em fórmulas infantis. De acordo com o FDA, ingredientes como leite em pó e concentrado de proteína de soro de leite serão analisados para identificar esporos de Clostridium botulinum. O objetivo é avaliar se a infecção bacteriana causadora do botulismo deve ser classificada como um risco previsível, permitindo que as empresas a integrem de forma proativa em seus procedimentos de inspeção. Como esses esporos nunca foram considerados contaminantes, os fabricantes de fórmulas infantis não eram obrigados a testá-los. As autoridades podem usar a análise para determinar os próximos passos.
As empresas podem ser obrigadas a verificar a presença de esporos de Clostridium botulinum. Não se sabe se houve alterações na produção desta fórmula infantil ligada ao surto ou se o risco de contaminação por essa bactéria foi ignorado ao longo do tempo. A Administração de Alimentos e Medicamentos dos EUA (FDA) espera obter a resposta por meio desta série de testes.
Não existem detalhes sobre a continuidade da fabricação da fórmula infantil pela ByHeart. A empresa não se pronunciou sobre o assunto, porém interrompeu as operações até que a investigação seja finalizada. A fábrica foi inspecionada pela FDA, porém o resultado não foi tornado público.
Conclusão
Neste caso único de botulismo infantil nos Estados Unidos, as autoridades estão realizando uma investigação conjunta sem precedentes. Ela envolve a FDA, o CDC, o IBTPP do CDPH, além de especialistas estaduais, locais e internacionais. Isso evidencia a necessidade de um esforço coletivo no enfrentamento ao botulismo. Também evidencia que o surto poderia ter sido internacional. Os dados foram divulgados de forma transparente em sites oficiais do governo dos Estados Unidos. A empresa de fórmula infantil ByHeart Whole Nutrition participa ativamente da pesquisa.
Em 2023, a FDA expressou preocupação com as áreas de produção de fórmulas infantis em pó ao enviar uma carta à indústria alertando sobre os riscos biológicos conhecidos ou razoavelmente previsíveis, como a bactéria Clostridium botulinum. Durante o atual surto e após a realização de testes especializados na fórmula infantil ByHeart, incluindo análises genéticas, o microrganismo identificado mostrou-se compatível com o C. botulinum presente no produto final. Isso indica que a contaminação detectada pode estar relacionada à cadeia de suprimentos e aos casos de botulismo registrados, sugerindo que a origem da contaminação pode estar na cadeia de suprimentos.
O desfecho ainda é desconhecido. As investigações continuam e não se sabe se a ByHeart pretende suspender a produção da fórmula. Também não se sabe se os fabricantes de fórmulas infantis em pó terão que realizar análises de C. botulinum a partir de agora, considerando-o um risco previsível. No entanto, é provável que as autoridades de padronização avaliem este risco nessas fórmulas. Cientificamente, o entendimento sobre o Clostridium botulinum está sendo expandido com o objetivo de minimizar riscos futuros e assegurar a segurança deste produto.
O surto foi rapidamente contido e não se espalhou além dos Estados Unidos, mesmo com o produto sendo vendido em 22 países. Não houve registro de casos internacionais. O governo se manifestou publicamente, orientando pais e responsáveis a descartar todos os lotes produzidos pela empresa em um recall internacional. Além disso, forneceu instruções aos médicos sobre como diagnosticar o botulismo, demonstrando seu compromisso com a população e a saúde pública. Foi rigoroso com os varejistas que continuavam vendendo o produto mesmo após o recolhimento. Reconheceu-se a ocorrência de um surto de botulismo infantil sem precedentes no país, uma vez que nenhum país encontra-se livre. No entanto, foi demonstrado um controle ágil e eficaz. As medidas são verdadeiramente inspiradoras para qualquer país do mundo, servindo como uma aula sobre botulismo e controle sanitário para quem quiser aprender. Obrigada pelo mergulho no tema!
Doralice Goes é mestranda em Segurança dos Alimentos pela UFSJ, sobreviveu ao botulismo alimentar em 2022 e, desde então, dedica-se ao estudo da doença, monitora casos globais, faz palestras na indústria e é autora de livro sobre o botulismo.
5 min leituraChegamos ao último post que nos coloca a par do maior surto de botulismo já registrado na história – apesar de ocorrer nos Estados Unidos, lembre-se de que o produto […]
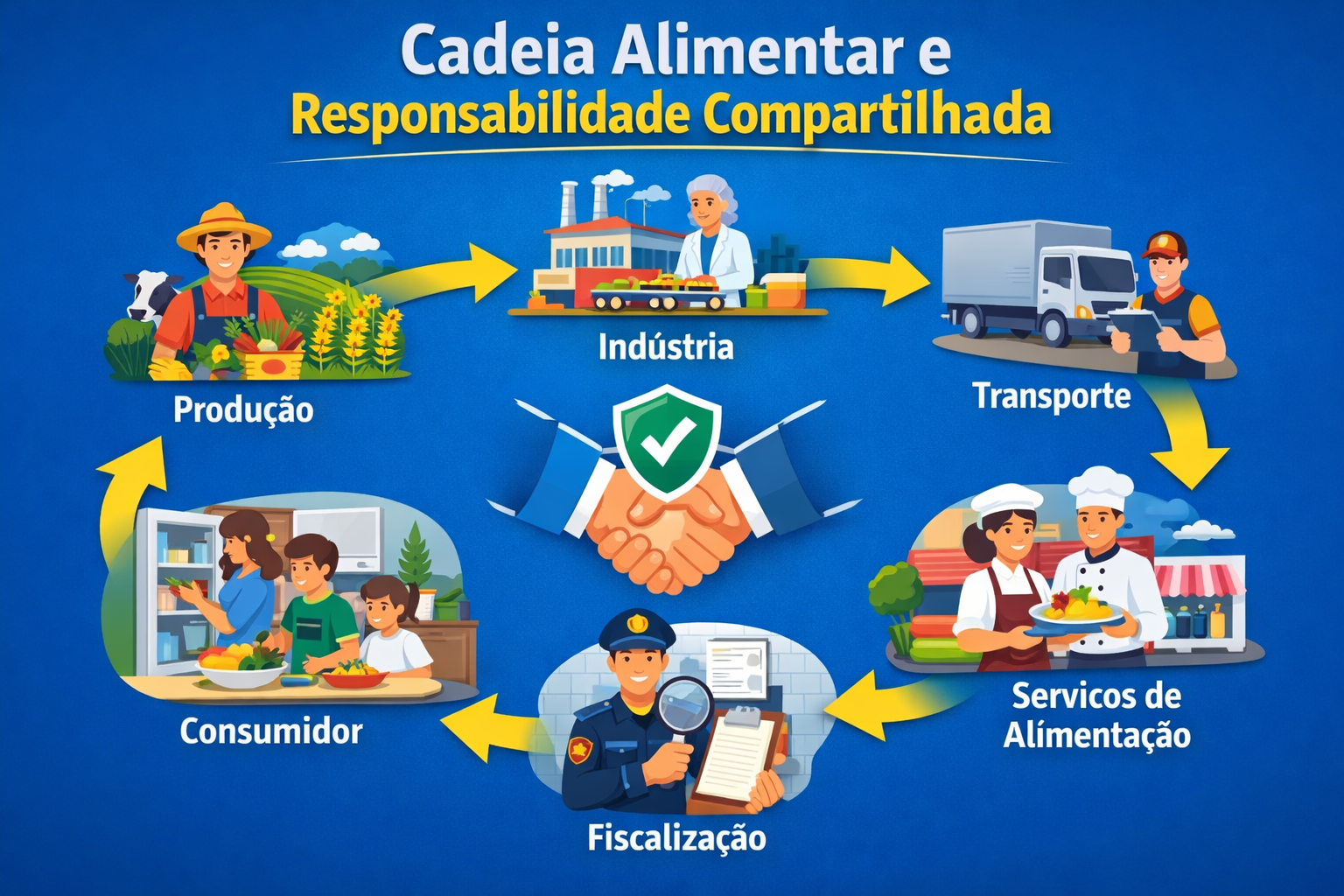
A cadeia alimentar reúne todas as etapas pelas quais o alimento passa, desde a produção até o consumo final. Nesse contexto, cada etapa influencia diretamente a segurança e a qualidade dos alimentos. Por esse motivo, a segurança de alimentos deve ser compreendida como uma responsabilidade compartilhada. Assim, todos os envolvidos exercem papel ativo na prevenção de riscos à saúde humana.
Produção primária
Na produção primária, agricultores e pecuaristas assumem a responsabilidade de adotar boas práticas agrícolas e pecuárias. Quando isso não ocorre, o uso inadequado de insumos, a água contaminada e o manejo incorreto de animais introduzem perigos nos alimentos. Consequentemente, essas falhas afetam toda a cadeia alimentar. Por outro lado, quando os produtores aplicam práticas seguras desde a origem, reduzem riscos e fortalecem sua responsabilidade.
Indústria de alimentos
A indústria ocupa posição central na cadeia alimentar e assume grande responsabilidade na transformação das matérias-primas. Para isso, aplica Boas Práticas de Fabricação e Programas de Pré-Requisitos. Além disso, utiliza sistemas de controle, como o APPCC. Da mesma forma, o atendimento a normas como a ISO 22000 e a FSSC 22000 reforça esse compromisso. Assim, a indústria demonstra responsabilidade ao controlar perigos, garantir rastreabilidade e monitorar processos.
Transporte e distribuição
No transporte e na distribuição, a responsabilidade está ligada à preservação das condições adequadas de higiene e temperatura. Quando ocorre a quebra da cadeia do frio, a segurança do alimento fica comprometida. Além disso, o transporte inadequado favorece o crescimento de micro-organismos. Portanto, transportadores e distribuidores precisam seguir procedimentos definidos. Dessa forma, asseguram que os alimentos cheguem ao destino em condições seguras.
Serviços de alimentação
Os serviços de alimentação desempenham papel essencial na cadeia alimentar. Nesse elo, restaurantes, padarias e cozinhas institucionais lidam diretamente com o preparo dos alimentos. Assim, gestores e manipuladores assumem grande responsabilidade. Além disso, a capacitação da equipe torna-se fundamental. Com isso, a higiene dos ambientes e o controle do preparo reduzem o risco de Doenças Transmitidas por Alimentos e reforçam a responsabilidade nesse setor.
Órgãos de fiscalização
Os órgãos de fiscalização e vigilância sanitária atuam como reguladores do sistema alimentar. Entre suas funções, elaboram legislações e realizam inspeções. Além disso, orientam os estabelecimentos e aplicam sanções quando necessário. Dessa maneira, fortalecem a responsabilidade compartilhada. Como resultado, incentivam o cumprimento das normas e a melhoria contínua da segurança de alimentos.
Responsabilidade do consumidor
O consumidor também tem responsabilidade importante na cadeia alimentar. Mesmo assim, práticas inadequadas no ambiente doméstico podem gerar riscos. Exemplos disso são o armazenamento incorreto e o cozimento insuficiente, que comprometem a segurança do alimento. Além disso, a contaminação cruzada representa perigo frequente. Portanto, ao adotar hábitos seguros, o consumidor fortalece a responsabilidade compartilhada e contribui para a prevenção de DTAs.
Integração da cadeia alimentar
A responsabilidade compartilhada exige integração entre todos os elos da cadeia alimentar. Quando um elo falha, todo o sistema sofre impacto. Por isso, cada participante precisa compreender o efeito de suas ações. Assim, essa visão integrada favorece a construção de uma cultura sólida de segurança de alimentos. Consequentemente, o comprometimento coletivo protege a saúde da população.
Em síntese, a cadeia alimentar depende da responsabilidade assumida em todas as etapas. Portanto, a segurança de alimentos não resulta de ações isoladas. Ao contrário, depende do esforço conjunto de produtores, indústria, distribuidores, serviços de alimentação, órgãos fiscalizadores e consumidores. Por fim, ao fortalecer a responsabilidade compartilhada, a sociedade promove a saúde pública e garante alimentos seguros e de qualidade.
2 min leituraA cadeia alimentar reúne todas as etapas pelas quais o alimento passa, desde a produção até o consumo final. Nesse contexto, cada etapa influencia diretamente a segurança e a qualidade […]
Estamos passando por um momento de crescente atenção da indústria e dos órgãos reguladores em torno de contaminantes formados durante processamentos térmicos de alimentos – entre eles, o 3-MCPD e seus ésteres. Exemplos disso são o código de práticas do Codex Alimentarius, o regulamento da União Europeia e o monitoramento conduzido pela FDA, além da recente inclusão deste contaminante na lista de monitoramento pela Anvisa.
Normalmente o 3-MCPD está associado a óleos vegetais, porém também se mostra potencialmente perigoso nas fórmulas infantis. Diante disso, como a indústria pode controlar esse contaminante de maneira eficaz?
O que é e qual o seu risco?
O 3-MCPDE (3-monocloropropano-1,2-diol éster) é uma molécula de éster que pode ocorrer em óleos vegetais após uma de suas etapas de produção. Durante o refino, o óleo é submetido a um processo térmico que tem como objetivo diminuir ou remover compostos que conferem sabor, odor e cor não esperados no produto terminado.
Esta molécula se transforma em 3-MCPD livre após hidrólise ácida no nosso trato digestivo. Segundo estudos realizados com roedores, o 3-MCPD causa efeitos adversos nos rins e órgãos reprodutores. Em 2013, a International Agency for Research on Cancer (IARC) classificou o 3-MCPD no grupo 2B, o que indica que é possivelmente carcinogênico para humanos.
O tema assume maiores proporções a partir do momento em que se sabe que óleos vegetais são ingredientes de proporções relevantes em fórmulas infantis. Isso levanta o alerta para a necessidade de aplicação de controles deste contaminante na indústria de alimentos, devido à vulnerabilidade deste público consumidor.
- Como mencionado pela colega Cíntia Malagutti, a Joint Expert Committee on Food Additives (JECFA) apresentou os resultados do estudo com as consequências da ingestão de 3-MCPDE e outros compostos, reforçando a necessidade de seu controle.
Com base nisso, a comissão do Codex Alimentarius preparou uma série de recomendações importantes para a indústria de óleos refinados e alimentos, por meio de um código de práticas. Este material inclui dicas que vão desde a agricultura, passando pelo refino, pós refino e medidas de processamento e que podem ser aplicadas de modo a reduzir os níveis de 3-MCPDE e éster glicidílico (GE) em alimentos.
Recomendações e estratégias de mitigação
Antes de passarmos essas orientações é importante saber:
De acordo com este código, as plantas absorvem durante seu desenvolvimento compostos clorados do solo, da água, de fertilizantes e outros. Esses compostos são precursores do 3-MCPDE.
A formação de GE inicia-se em torno de 200°C, com maior taxa a partir de 230°C. Enquanto que a formação de 3-MCPDE ocorre na faixa de 160 – 200°C, não aumentando com o aumento da temperatura.
Devido a seus diferentes mecanismos de formação, as estratégias de mitigação tendem a ser diferentes. No caso do GE, que é formado com temperaturas mais altas, a estratégia é o controle da alta temperatura. Apesar disso, diminuir a temperatura pode alcançar a faixa de formação do 3-MCPDE.
As recomendações indicam combinar medidas para garantir maior efetividade das ações. Essa combinação pode incluir estratégias como a minimização do uso de fertilizantes, pesticidas e água que apresentam excesso de compostos com cloro.
Especificamente no caso de óleo de frutos como a palma, recomenda-se realizar a colheita no momento mais adequado, ou seja, quando apresentam menor concentração da enzima lipase, associada ao processo de formação de 3-MCPDE.
Na indústria, as recomendações envolvem o armazenamento de grãos em temperaturas inferiores a 25°C, com umidade menor que 7%, na busca dos menores índices da enzima lipase. Além disso, recomenda-se monitorar precursores como DAGs (diacilglicerois), FFAs (ácidos graxos livres) e compostos clorados nas etapas de produção do óleo bruto.
Já na etapa de branqueamento, indica-se utilizar maiores quantidades de terra branqueadora, além de evitar aquelas terras que apresentam quantidades significativas de compostos com cloro.
Na desodorização, o ideal para óleos vegetais é manter a faixa de 190 a 230°C. Além disso, recomenda-se aplicar vácuo mais forte para facilitar a remoção dos compostos voláteis, de modo a não ser necessário o aumento da temperatura, o que favoreceria a formação de GE.
- Todas essas medidas e outras estão disponíveis no material do Codex Alimentarius de 2019 (código de referência CXC 79-2019).
No caso de indústrias alimentícias, como as de fórmulas infantis, é importante utilizar óleo com as menores concentrações de 3-MCPDE e GE, de modo a evitar a concentração deste contaminante em seu produto terminado. Isso se dá com o devido processo de homologação de fornecedores, bem como medidas de controle para o recebimento de matérias-primas.
O monitoramento e regulamentações
O FDA estabeleceu métodos laboratoriais de monitoramento de 3-MCPDE e GE, inicialmente com foco nas fórmulas infantis. Entre os anos de 2013 e 2016 foram avaliadas 98 amostras de fórmulas. A partir de então, o órgão iniciou conversas com o segmento industrial para apresentar suas preocupações.
Na sequência, entre 2017 e 2019, com o objetivo de avaliar se os fabricantes reduziram o nível de 3-MCPDE e GE nas fórmulas infantis, novas 222 amostras foram avaliadas, sendo que 3 fabricantes apresentaram sucesso na redução.
Já entre 2021 e 2023, outras 206 amostras foram analisadas, o que indicou que todos os 4 fabricantes avaliados reduziram o nível dos referidos contaminantes a níveis consistentes internacionalmente.
Apesar dos limites não serem definidos na legislação estadunidense, a União Europeia define tais limites claramente para óleo, gorduras e alimentos para lactentes através do Regulamento (EU) 2023/915.
Já no Brasil, a ANVISA publicou em março de 2025 a IN 351 que complementa a IN 160 de 2022. Ela estabelece limites máximos tolerados de contaminantes em alimentos, incluindo o 3-MCPD. Porém, por enquanto este contaminante está indicado apenas para condimentos líquidos contendo proteínas vegetais hidrolisadas ácidas, com prazo de implementação findando em março de 2026.
Notícias recentes indicam a ocorrência e a relevância desses controles não apenas nos óleos, gorduras e alimentos infantis. Em julho de 2025, a Coreia procedeu um recall de molhos de soja devido ao alto índice de 3-MCPD em sua composição.
Importante reforçar que o 3-MCPD e seus ésteres não são inevitáveis, uma vez que o controle é possível aplicando uma gestão adequada e focada. Além disso, um trabalho preventivo e sistêmico iniciando na agricultura tende a minimizar os impactos na indústria.
Essas estratégias vão ao encontro da tendência percebida globalmente no monitoramento deste contaminante. Assim, a indústria que alia a ciência, a tecnologia e um sistema de gestão direcionado garante não apenas conformidade com a legislação, como também abertura em um mercado cada dia mais exigente e informado.
Imagem: Kaboompics
4 min leituraEstamos passando por um momento de crescente atenção da indústria e dos órgãos reguladores em torno de contaminantes formados durante processamentos térmicos de alimentos – entre eles, o 3-MCPD e […]
A regulamentação de aditivos alimentares e coadjuvantes de tecnologia varia significativamente entre países, refletindo diferenças nos modelos de avaliação de risco, no grau de aplicação do princípio da precaução e em fatores culturais, econômicos e históricos.
Embora exista convergência conceitual sobre segurança dos alimentos, as decisões regulatórias frequentemente divergem quanto ao momento e à intensidade das restrições aplicadas a determinadas substâncias.
No âmbito regulatório:
- Aditivo alimentar é toda substância adicionada intencionalmente aos alimentos com a finalidade de modificar ou manter suas características físicas, químicas, biológicas ou sensoriais, como cor, sabor, aroma, textura, estabilidade ou conservação, passando a exercer função tecnológica no produto final e, portanto, sendo considerada parte integrante da formulação do alimento;
- Coadjuvante de tecnologia de fabricação é uma substância utilizada durante etapas específicas do processamento industrial com o objetivo de facilitar ou viabilizar operações tecnológicas, como extração, clarificação, filtração ou fermentação, não sendo destinada ao consumo direto nem a desempenhar função tecnológica no alimento final, embora possa deixar resíduos tecnicamente inevitáveis, desde que seguros e dentro dos limites estabelecidos pela legislação sanitária.
No Brasil, o uso de aditivos alimentares e coadjuvantes de tecnologia é regulado principalmente pela Agência Nacional de Vigilância Sanitária (Anvisa), com base em listas positivas, que definem quais substâncias podem ser utilizadas, suas funções tecnológicas, categorias de alimentos autorizadas e limites máximos de uso.
A base legal vigente inclui a RDC nº 778/2023 e a Instrução Normativa nº 211/2023, atualizadas por atos normativos posteriores da própria Anvisa.
Esse modelo regulatório exige que o aditivo ou coadjuvante esteja expressamente autorizado para uma categoria específica de alimento, não sendo admitido o uso por analogia ou extrapolação tecnológica.
A Anvisa adota como referência técnica avaliações conduzidas no âmbito do Codex Alimentarius, da Organização Mundial da Saúde (OMS), da FAO, bem como, de forma complementar, pareceres e avaliações de agências reguladoras internacionais, como a Autoridade Europeia de Segurança de Alimentos (EFSA) e a Food and Drug Administration (FDA) dos Estados Unidos.
No entanto, o Brasil não incorpora automaticamente decisões regulatórias estrangeiras, o que resulta em situações nas quais determinadas substâncias permanecem autorizadas no país enquanto já foram proibidas ou severamente restringidas em outras jurisdições.
Na União Europeia, a abordagem regulatória é fortemente baseada no princípio da precaução.
Isso significa que, diante de incertezas científicas relevantes sobre a segurança de uma substância, um aditivo pode ser proibido mesmo na ausência de comprovação definitiva de dano à saúde humana.
Esse modelo ficou particularmente evidente no caso do dióxido de titânio (E171), amplamente utilizado como agente de cor branca em confeitos, sobremesas e outros produtos alimentícios.
Em 2021, a EFSA concluiu que não era possível excluir um potencial efeito genotóxico do dióxido de titânio, ou seja, sua capacidade de causar danos ao DNA. Diante da impossibilidade de estabelecer um nível seguro de ingestão, a Comissão Europeia optou pelo banimento total do aditivo em alimentos a partir de 2022.
No Brasil, por outro lado, o dióxido de titânio ainda figura como aditivo autorizado em determinadas categorias de alimentos, desde que atendidas as especificações de pureza e as condições de uso estabelecidas pela Anvisa. Nos Estados Unidos, o composto também permanece permitido pela FDA.
Esse cenário ilustra claramente a diferença de abordagem entre os sistemas regulatórios: enquanto a União Europeia opta por eliminar o risco potencial diante da incerteza científica, Brasil e Estados Unidos mantêm o aditivo autorizado até que haja evidência mais conclusiva de dano em condições reais de consumo.
Outro exemplo relevante envolve o bromato de potássio, um agente oxidante historicamente utilizado na panificação para melhorar a elasticidade da massa e o volume do pão. A substância é classificada como possivelmente carcinogênica com base em estudos toxicológicos, motivo pelo qual foi banida na União Europeia há décadas.
No Brasil, o uso de bromato de potássio já foi permitido no passado, mas atualmente encontra-se proibido, alinhando-se à posição europeia.
Nos Estados Unidos, o bromato de potássio permanece tecnicamente permitido em âmbito federal, embora seu uso seja cada vez mais raro, amplamente evitado pela indústria e sujeito a restrições comerciais, regulatórias e de mercado.
Os corantes artificiais representam um dos grupos com maior divergência regulatória internacional.
A eritrosina (INS 127; FD&C Red No. 3), por exemplo, é um corante vermelho utilizado em confeitos, gelatinas e frutas em calda. Estudos experimentais levantaram preocupações relacionadas a efeitos sobre a tireoide e potencial carcinogenicidade em modelos animais.
Na União Europeia, o uso é extremamente restrito, enquanto no Brasil o corante ainda consta nas listas de aditivos permitidos para aplicações específicas, sempre respeitando limites máximos de uso estabelecidos pela legislação.
Nos Estados Unidos, a FDA determinou a retirada progressiva da eritrosina para uso alimentar, com restrições cada vez mais severas e eliminação prevista em etapas.
O caso do amaranto (INS 123) ilustra uma situação inversa. Esse corante vermelho foi banido nos Estados Unidos desde a década de 1970, após estudos sugerirem associação com tumores em animais.
A União Europeia, entretanto, manteve o amaranto autorizado em níveis muito controlados, e o Brasil também permite seu uso em categorias específicas de alimentos.
Esses exemplos demonstram que as decisões regulatórias nem sempre convergem globalmente e podem seguir caminhos distintos ao longo do tempo, mesmo diante do mesmo conjunto de evidências científicas.
No que se refere aos coadjuvantes de tecnologia, as diferenças regulatórias são menos perceptíveis ao consumidor, mas igualmente relevantes do ponto de vista técnico.
Solventes de extração, agentes de clarificação e auxiliares de processamento podem ser autorizados no Brasil com base na premissa de que não exercem função tecnológica no produto final e deixam apenas resíduos tecnicamente inevitáveis.
Em alguns casos, determinadas substâncias desse grupo foram reavaliadas e posteriormente banidas na União Europeia por preocupações toxicológicas ou ambientais, enquanto permanecem permitidas no Brasil sob limites residuais específicos, definidos com base em avaliações de risco.
Essas divergências regulatórias decorrem, em grande parte, dos diferentes critérios de aceitabilidade do risco adotados por cada jurisdição.
- A União Europeia privilegia a eliminação preventiva de substâncias potencialmente perigosas, mesmo quando o risco não está plenamente caracterizado;
- Os Estados Unidos adotam um modelo mais permissivo, exigindo evidência clara de dano em condições normais de consumo antes de restringir ou proibir um aditivo, frequentemente utilizando o conceito de substâncias GRAS (Generally Recognized As Safe);
- O Brasil, por sua vez, segue um modelo intermediário, baseado em listas positivas e análise de risco, mas sem incorporar automaticamente todas as decisões mais restritivas adotadas pela UE.
Os nitritos ocupam uma posição particular na regulamentação de alimentos, pois, embora também atuem durante o processamento, são classificados como aditivos alimentares, e não como coadjuvantes de tecnologia.
O nitrito de sódio e o nitrito de potássio são adicionados intencionalmente a produtos cárneos curados para exercer funções tecnológicas no alimento final, como a fixação da cor característica, o desenvolvimento do sabor típico e, sobretudo, a inibição do crescimento de Clostridium botulinum, agente causador do botulismo.
Por desempenharem essas funções diretamente no produto consumido, os nitritos integram a formulação do alimento e estão sujeitos a limites máximos rigorosos, definidos com base em avaliações toxicológicas que reconhecem o risco potencial de formação de nitrosaminas, compostos associados a efeitos carcinogênicos em determinadas condições.
No Brasil, na União Europeia e nos Estados Unidos, os nitritos permanecem autorizados, porém sob regimes regulatórios cuidadosamente controlados.
- No Brasil, a Anvisa permite seu uso exclusivamente em produtos cárneos específicos, com limites alinhados ao Codex Alimentarius e exigência de boas práticas de fabricação para minimizar riscos;
- Na União Europeia, após sucessivas reavaliações da EFSA, os limites foram reduzidos e tornaram-se mais restritivos por categoria de produto, refletindo a aplicação do princípio da precaução, ainda que o aditivo seja mantido devido ao seu papel essencial na segurança microbiológica;
- Nos Estados Unidos, a FDA e o USDA também autorizam os nitritos, com limites legais definidos, exigências de rotulagem e, frequentemente, a obrigatoriedade de uso combinado com antioxidantes, como ascorbato ou eritorbato, justamente para reduzir a formação de nitrosaminas.
Do ponto de vista técnico e regulatório, é incorreto afirmar que a simples autorização de um aditivo no Brasil signifique negligência sanitária. Em geral, essas substâncias são permitidas com base nas melhores avaliações toxicológicas disponíveis à época da regulamentação.
No entanto, também é inegável que o Brasil, em alguns casos, revisa ou atualiza suas listas de forma mais lenta quando comparado a jurisdições que aplicam de maneira mais rigorosa o princípio da precaução.
Conclui-se, portanto, que existem aditivos alimentares e coadjuvantes de tecnologia autorizados no Brasil que já foram proibidos ou severamente restringidos na União Europeia e, em alguns casos, nos Estados Unidos. Essas diferenças refletem escolhas regulatórias distintas, especialmente quanto ao nível de precaução adotado frente à incerteza científica.
Para a indústria de alimentos, isso implica a necessidade de atenção constante à legislação internacional, sobretudo quando há interesse em exportação, e para o consumidor e o formulador técnico, reforça a importância da atualização contínua baseada em evidências científicas e decisões regulatórias globais.
5 min leituraA regulamentação de aditivos alimentares e coadjuvantes de tecnologia varia significativamente entre países, refletindo diferenças nos modelos de avaliação de risco, no grau de aplicação do princípio da precaução e […]
Sejam bem-vindos à segunda parte da trilogia sobre o surto incomum de botulismo infantil que atinge os Estados Unidos (para ler o primeiro post, clique aqui).
A seguir, examinaremos a composição da fórmula infantil, os resultados da análise laboratorial, o fabricante da fórmula e como os Estados Unidos supervisionam a fabricação desse produto.
Análise na fórmula infantil
A empresa e o FDA começaram a testar o produto, e os resultados iniciais do laboratório divulgados pelo CDPH indicaram a presença de Clostridium botulinum em uma lata aberta da fórmula infantil fornecida a um bebê diagnosticado com botulismo. A ByHeart comunicou que análises laboratoriais independentes, conduzidas nas amostras de produtos de fórmula infantil lacrados e mantidos em suas instalações, detectaram a presença de Clostridium botulinum. A maioria das amostras analisadas pela FDA apresentou resultado preliminar negativo quanto à presença da bactéria, e todos os resultados positivos em produtos finalizados começaram a ser comunicados. Desde 10 de dezembro de 2025, não houve registro de nenhum novo caso.
Em seguida, a ByHeart divulgou resultados positivos para Clostridium botulinum em seis das 36 amostras do produto final, coletadas de dois lotes que estavam no recall inicial do produto. Em 26 de janeiro de 2025, foi determinada a origem da contaminação em cepa de um ingrediente; no entanto, tanto a FDA quanto os CDC não divulgaram o nome do fabricante.
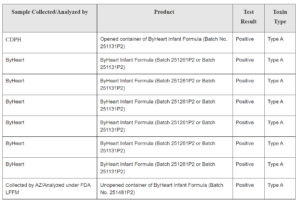
Em 23 de janeiro de 2026, a FDA confirmou que duas amostras apresentaram resultado positivo para Clostridium botulinum tipo A. A primeira amostra, obtida de uma embalagem selada de fórmula infantil da ByHeart, foi submetida à análise de sequenciamento de genoma completo (WGS). Os resultados mostraram que a bactéria identificada é geneticamente idêntica ao microrganismo isolado de um bebê internado durante o surto. Além disso, corresponde a dois isolados encontrados em leite em pó integral, ingrediente usado na fabricação da fórmula e previamente analisado pela empresa. A segunda amostra foi obtida de um fornecedor da ByHeart e examinada pelo Laboratório Wadsworth, localizado em Nova York. De acordo com a análise genética, o microrganismo encontrado é compatível com o Clostridium botulinum identificado no produto final da fórmula infantil da ByHeart. Isso reforça a conexão entre a contaminação detectada no produto e a cadeia de suprimentos.
As análises confirmam que a contaminação tem origem na cadeia de suprimentos, e provavelmente é ligada ao leite em pó integral. Isso possibilita que as autoridades façam uma ligação científica entre o bebê enfermo, o produto ingerido, o componente e o fornecedor. Apesar de esses resultados melhorarem o entendimento da FDA sobre o surto, a investigação prossegue para identificar a origem da contaminação. No entanto, a detecção de C. botulinum em fórmulas infantis ou em seus componentes é complexa, e os resultados podem demorar várias semanas. Os esporos termorresistentes necessitam de uma ativação específica para serem identificados, e os exames para esta bactéria em fórmulas infantis são especializados, com resultados finais que demandam testes confirmatórios. Ademais, há um número restrito de laboratórios que possuem equipamentos e recursos especializados.
Quem é a ByHeart e quais são os componentes da sua fórmula infantil?
Estabelecida em 2016 pelos irmãos Mia Funt e Ron Belldegrun, com sede em Nova York, a empresa lançou sua primeira fórmula infantil em março de 2022, durante uma escassez desse produto nos Estados Unidos. A companhia foi a primeira nova fabricante de fórmulas infantis registrada pela FDA em mais de 15 anos. A fórmula infantil Whole Nutrition da ByHeart é composta por uma combinação de proteínas patenteada, desenvolvida para imitar o leite materno humano, utilizando leite integral orgânico de vacas alimentadas em pasto. Ele possui lactoferrina, alfa-lactalbumina, uma relação de 80:20 entre soro e caseína similar à do colostro, lactose como único carboidrato, proteínas parcialmente hidrolisadas, prebióticos orgânicos e os ácidos graxos DHA e ARA. A fórmula não contém xarope de milho, glúten, transgênicos, maltodextrina, soja, DHA extraído de hexano, hormônios artificiais de crescimento nem óleo de palma.
A fórmula tinha como objetivo promover a inovação necessária no mercado de nutrição infantil de próxima geração – o futuro da nutrição. Ela oferecia melhorias como digestão mais simplificada, redução de regurgitação, ganho de peso mais eficiente e desenvolvimento cerebral. Além disso, recebeu milhões em financiamento. Em 2022, a empresa lançou uma plataforma própria para suporte à nutrição e alimentação.
Entre 2023 e 2024, a ByHeart expandiu rapidamente sua presença no varejo americano, passando por redes como Target, Whole Foods Market, Wegmans, Publix e Walmart, até atingir quase 12 mil pontos de venda. Em dezembro de 2024, a companhia fortaleceu sua governança com a inclusão de Denice Torres, ex-executiva da Johnson & Johnson, no conselho. Em maio de 2025, foi lançada a embalagem portátil para alimentação infantil chamada “Anywhere Pack”. De acordo com a FDA, embora os produtos da ByHeart sejam amplamente distribuídos, eles correspondem a menos de 1% do mercado de fórmulas infantis nos EUA.
Apesar de ter sido a primeira fórmula infantil nos EUA a conquistar o Prêmio de Pureza do Clean Label Project, que analisa produtos para identificar mais de 500 possíveis contaminantes, como metais pesados e pesticidas, sua fórmula esteve envolvida em outro caso de contaminação bacteriana em 2022. O contaminante foi o Cronobacter sakazakii, responsável por infecções graves e potencialmente fatais, como sepse ou meningite. A companhia efetuou um recall voluntário de cinco lotes da fórmula. Não houve registro de reclamações de consumidores relacionadas a doenças.
Entre dezembro de 2022 e fevereiro de 2023, a FDA inspecionou as instalações da ByHeart em Reading, Pensilvânia, assim como as da Mead Johnson Nutrition (Reckitt) e da Perrigo Wisconsin, LLC. Após as inspeções, foram emitidas cartas de advertência mencionando violações das normas relacionadas a fórmulas infantis. No entanto, a FDA não recomendou que pais e cuidadores descartassem ou evitassem a compra de nenhuma fórmula infantil específica. A agência não teve conhecimento de nenhum produto distribuído em que a contaminação tenha sido confirmada e considera que os recalls foram eficientes para retirar os lotes possivelmente contaminados do mercado.
A advertência indicou que a fábrica apresentava condições insalubres e apontou falhas no programa de monitoramento ambiental da instalação. Isso incluía vazamentos de águas provenientes de fora do prédio, que se dirigiam às áreas de produção por meio de uma clarabóia instalada no telhado da sala de processamento, onde o produto testou positivo para Enterobacter Sakazakii. Além disso, foi detectado outro vazamento no selante ao redor da persiana da torre de secagem, com a presença de Cronobacter spp.
Os relatórios de inspeção da Food and Drug Administration apontaram problemas graves no local da empresa nesta fábrica. Além do vazamento no telhado, foi identificado mofo em um tanque destinado à água limpa. Em 11 de dezembro de 2023, um inspetor notou que “moscas zumbiam acima de uma área crítica da produção de fórmulas”. Na mesma região, o inspetor registrou a presença de mais de 2.500 insetos voadores mortos próximos a três armadilhas de luz destinadas a insetos. Além disso, de acordo com o relatório, a fábrica descumpriu suas normas de manutenção das temperaturas essenciais para eliminar bactérias da fórmula antes de enviá-la para embalagem. No entanto, não houve notificação e a fórmula foi enviada aos clientes. A inspeção foi classificada pela FDA como tendo o mais alto nível de preocupação.
Em uma carta datada de 8 de março de 2023, a FDA expressou preocupação com as áreas de produção de fórmulas infantis em pó. Destacou que os fabricantes devem identificar e levar em consideração todos os riscos biológicos conhecidos ou razoavelmente previsíveis, incluindo a bactéria Clostridium botulinum. A Byheart foi mencionada na carta de advertência em razão da inspeção realizada em fevereiro de 2023. Em 30 de agosto de 2023, a empresa recebeu outra advertência e apresentou diversos planos de ação corretiva em resposta.
Como a FDA supervisiona a segurança e a qualidade nutricional das fórmulas infantis?
A produção de fórmulas infantis nos Estados Unidos é regulamentada pela FDA, garantindo a segurança desses produtos. Fórmulas infantis constituem uma opção ao leite materno para a alimentação de bebês de até 12 meses, podendo ser o alimento exclusivo, sendo que a maioria dos bebês nos EUA depende dessas fórmulas para sua nutrição.
Os produtores de fórmulas infantis precisam atender às exigências pertinentes da Lei Federal de Alimentos, Medicamentos e Cosméticos (Federal Food, Drug, and Cosmetic Act) e às que estão presentes nos regulamentos de implementação da FDA. Um fabricante que deseja vender uma nova fórmula infantil nos Estados Unidos precisa registrá-la, notificá-la e enviar à FDA uma declaração escrita atestando sua conformidade com as regulamentações.
Apesar de a Agência não aprovar fórmulas infantis, ela é responsável por analisar os requisitos quando notificada pelos fabricantes antes da venda. Esses requisitos abrangem segurança, adequação nutricional, embalagem e rotulagem. Quando não se aplica, a fórmula pode ser considerada alterada, rotulada de forma inadequada ou ambas as opções, e, nesse caso, pode ser sujeita a medidas coercitivas, como o recolhimento obrigatório. Aproximadamente 30 nutrientes devem estar presentes em quantidades mínimas, enquanto 10 deles devem estar em quantidades máximas. Além disso, qualquer um deles deve ser seguro e apropriado para esse propósito.
Além disso, há exigências específicas para rotular fórmulas infantis, e a agência realiza inspeções anuais nas instalações das fábricas. Todos os produtos de fórmula infantil comercializados nos Estados Unidos, tanto os fabricados internamente quanto os importados, precisam cumprir todas as normas americanas. As autoridades desaconselham o uso de fórmulas caseiras, pois elas podem aumentar o risco de contaminação ou não fornecer a quantidade adequada de cálcio.
A agência está cooperando com os fabricantes, que agora precisam ter planos de contingência para riscos.
Doralice Goes é mestranda em Segurança dos Alimentos pela UFSJ, sobreviveu ao botulismo alimentar em 2022 e, desde então, dedica-se ao estudo da doença, monitora casos globais, faz palestras na indústria e é autora de livro sobre o botulismo.
6 min leituraSejam bem-vindos à segunda parte da trilogia sobre o surto incomum de botulismo infantil que atinge os Estados Unidos (para ler o primeiro post, clique aqui). A seguir, examinaremos a […]
Um dos requisitos fundamentais para o êxito de qualquer sistema de gestão da segurança de alimentos é a comunicação eficaz.
A raiz de muitos problemas observados nas unidades produtoras de alimentos está, justamente, nas falhas de comunicação entre as partes envolvidas — emissores, interlocutores e receptores. Se já é desafiador manter uma comunicação clara e eficiente entre profissionais que compartilham o mesmo idioma, esse desafio torna-se ainda maior quando envolve trabalhadores estrangeiros, que não dominam plenamente a língua local.
O Brasil é reconhecido como um dos países mais diversos do mundo, característica reforçada pelo aumento significativo da imigração internacional nas últimas décadas. Dados de órgãos oficiais, como o IBGE e o Observatório das Migrações Internacionais (OBMigra), indicam que, especialmente a partir da década de 2010, o país passou a receber um fluxo expressivo de imigrantes haitianos e, mais recentemente, venezuelanos. Grande parte desses trabalhadores foi absorvida por setores que demandam mão de obra intensiva, como a indústria de alimentos, frigoríficos, agroindústrias e serviços associados à cadeia produtiva de alimentos.
Os haitianos começaram a chegar em maior número ao Brasil após o terremoto de 2010, sendo direcionados principalmente para regiões industriais e agroindustriais. Já a imigração venezuelana se intensificou a partir de 2017, em decorrência da crise humanitária no país vizinho. Em ambos os casos, observa-se que a maioria desses profissionais não possui fluência em língua portuguesa, o que impõe desafios adicionais para a integração no ambiente industrial.
A absorção dessa mão de obra estrangeira representa uma oportunidade social e econômica, tanto para os imigrantes quanto para o país. No entanto, um aspecto ainda pouco discutido é a eficiência da comunicação com esses profissionais no contexto da segurança de alimentos. As barreiras linguísticas podem comprometer o entendimento de políticas da qualidade, programas de segurança de alimentos, instruções de trabalho, procedimentos operacionais padronizados (POPs), boas práticas de fabricação (BPFs) e treinamentos obrigatórios.
Na indústria de alimentos, onde a rotina é intensa e os riscos são elevados, a comunicação inadequada pode resultar em falhas operacionais, desvios de processo, contaminações e não conformidades graves. Muitas vezes, o ritmo acelerado da produção não permite um acompanhamento individualizado capaz de avaliar o real nível de compreensão e percepção dos colaboradores estrangeiros. Nessas situações, falhas recorrentes podem ser erroneamente interpretadas como desatenção ou negligência, quando, na verdade, estão associadas à dificuldade de compreensão do idioma e da cultura organizacional local.
Diante desse cenário, torna-se essencial que as empresas adotem estratégias de monitoramento contínuo do entendimento e da aprendizagem destes colaboradores. A comunicação eficaz é um pilar estratégico para garantir a segurança dos alimentos, a conformidade legal, a redução de riscos e a construção de uma cultura organizacional sólida e inclusiva.
Sugestões para melhorar a comunicação com profissionais estrangeiros na indústria de alimentos
- Utilizar materiais visuais, como cartazes ilustrativos, pictogramas, fluxogramas e vídeos demonstrativos, reduzindo a dependência exclusiva da linguagem escrita;
- Adaptar treinamentos com linguagem simples, objetiva e, sempre que possível, com apoio de tradutores ou mediadores bilíngues;
- Desenvolver materiais fundamentais (regras básicas, higiene pessoal, segurança de alimentos e procedimentos críticos) em mais de um idioma, especialmente espanhol e francês/creole haitiano;
- Realizar avaliações periódicas de entendimento, por meio de observações práticas, simulações e diálogos diretos no ambiente de trabalho;
- Capacitar líderes e supervisores para uma comunicação intercultural, promovendo empatia, paciência e escuta ativa;
- Incentivar programas internos de alfabetização ou ensino básico de português voltados ao contexto industrial;
- Promover a integração cultural, criando um ambiente mais acolhedor, no qual o colaborador estrangeiro se sinta seguro para tirar dúvidas e pedir orientações.
Investir em comunicação eficaz com profissionais estrangeiros não é apenas uma ação de responsabilidade social, mas uma estratégia fundamental para a segurança de alimentos, a eficiência operacional e a sustentabilidade das indústrias alimentícias em um contexto cada vez mais globalizado.
Leia também:
Cinco sugestões para melhorar a comunicação da segurança de alimentos com o chão de fábrica
3 min leituraUm dos requisitos fundamentais para o êxito de qualquer sistema de gestão da segurança de alimentos é a comunicação eficaz. A raiz de muitos problemas observados nas unidades produtoras de […]
Falar de rotulagem de alimentos costuma remeter imediatamente a listas, normas, porcentagens e exigências legais. Para muitos, é um tema técnico demais. Para outros, apenas mais uma obrigação a ser cumprida. Esta série de artigos parte de uma pergunta diferente:
“para quem, de fato, a rotulagem existe?”
Ao longo dos próximos artigos, a rotulagem será abordada não apenas como um requisito regulatório, mas como uma ferramenta de comunicação, prevenção e cuidado, especialmente em contextos onde o alimento se afasta de quem o produziu e a informação deixa de acompanhar o que será consumido.
A proposta não é esgotar legislações nem transformar o leitor em especialista, mas construir consciência. Questionar por que, mesmo com normas claras, a informação nem sempre chega a quem precisa dela. E por que cumprir a lei, muitas vezes, não é suficiente para garantir escolhas seguras.
Esta série parte de uma provocação inicial, a ideia de que o cumprimento legal estabelece um mínimo e segue avançando para os diferentes cenários onde a rotulagem se tensiona na prática: a indústria, o delivery, festas, eventos, doações e outras situações em que o alimento circula sem contexto.
Mais do que explicar o que deve constar em um rótulo, os textos convidam produtores, comerciantes e consumidores a refletir sobre como a informação circula, quem realmente a acessa e em que momento ela faz diferença.
“A rotulagem, aqui, não é tratada como papel. É tratada como cultura.”
Porque talvez o avanço da rotulagem não esteja em criar mais regras, mas em criar mais consciência. E quando a informação passa a ser vista como cuidado, e não apenas como obrigação, o alimento deixa de ser apenas seguro. Ele passa a ser responsável.
Temas que essa série de artigos irá explorar
Sem antecipar respostas prontas, esta série irá percorrer temas como:
- a diferença entre cumprir requisitos e comunicar riscos;
- os limites da rotulagem no delivery;
- o alimento fora do controle de quem produziu, em festas, eventos e doações;
- a leitura crítica do rótulo por quem consome;
- e, futuramente, reflexões sobre por que alguns países adotam abordagens mais humanas e acessíveis na rotulagem do que outros, além do papel dos sistemas de gestão de segurança de alimentos nesse processo.
Cada artigo pode ser lido de forma independente, mas todos se conectam por uma ideia central: informação só protege quando circula. Vamos nessa?
A informação que acompanha o alimento
Parte 1: estamos rotulando para cumprir a lei ou para cuidar?
“Quando o rótulo existe, mas a informação não chega, parte essencial da cultura sanitária fica pelo caminho.”
Este artigo integra uma série dedicada a discutir a rotulagem de alimentos não apenas como exigência regulatória, mas como instrumento de comunicação, prevenção e cuidado. A proposta não é esgotar o tema, mas provocar reflexão sobre como a informação circula ou deixa de circular quando o alimento se afasta de quem o produziu.
O começo: o conforto do requisito cumprido
Existe um alívio silencioso quando um rótulo está “em conformidade”. A sensação de dever cumprido. A ideia de que, dali em diante, o risco “não é mais nosso.” No mundo ideal da rotulagem, esse alívio faria sentido. O alimento sai da produção:
- com denominação de venda correta,
- lista de ingredientes completa,
- alergênicos declarados,
- tabela nutricional adequada,
- validade definida.
“A legislação de rotulagem estabelece critérios técnicos mínimos para garantir o direito à informação e reduzir riscos ao consumidor.”
No papel, tudo está certo. Mas o papel não come, não escolhe e não adoece.
Quando o alimento entra no mundo real

A rotulagem não diz:
- se alguém vai ler,
- se alguém vai entender,
- se a informação chega no momento certo,
- se quem consome é quem recebeu o rótulo.
O meio do arco: a ilusão da informação “disponível”
Um dos pontos menos questionados e mais frágeis da prática cotidiana é a ideia de que a informação pode ser fornecida quando solicitada. Na teoria, isso resolve. Na prática, cria uma cadeia improvável.
“Para que a informação verbal seja segura, quem informa precisa conhecer profundamente a formulação, os ingredientes e os riscos associados ao alimento.”
Quem serve:
- nem sempre produziu;
- nem sempre conhece a receita;
- nem sempre sabe identificar perigos a segurança de alimentos, como por exemplo, alergênicos indiretos;
- nem sempre entende a diferença entre “não contém” e “não foi adicionado”.
Quem consome:
- nem sempre sabe o que perguntar;
- nem sempre reconhece o risco;
- nem sempre está em condição de escolher.
Ou seja, a informação existe, mas não circula.
Quando o rótulo vira documento, não comunicação

Outro ponto sensível: a rotulagem, aos poucos, foi sendo tratada como prova de conformidade, não como ferramenta de diálogo. Cumpre-se o requisito. Valida-se o modelo. Segue-se o processo.
“Ter um rótulo correto não significa que o risco foi controlado. Significa apenas que um requisito foi cumprido.”
Rotulagem é uma ferramenta de comunicação de risco. Quando essa função se perde, o rótulo vira apenas um artefato burocrático. Nesse cenário, o rótulo protege mais quem produziu do que quem consome. E isso deveria nos incomodar.
Não é a legislação que falha
Há uma tentação constante de dizer que “a lei é insuficiente”. Mas talvez a pergunta correta seja outra.
“Não é a legislação que falha, é a expectativa de que ela resolva sozinha o que é cultural.”
Nenhuma RDC ensina empatia. Nenhuma instrução normativa cria consciência. Nenhuma obrigação legal substitui a responsabilidade. A lei organiza. Mas somente a cultura sustenta.
Boas práticas começam onde a norma termina
Boas práticas nascem quando alguém faz perguntas que não estão escritas:
- Isso está claro para quem vai consumir?
- Essa informação chega junto com o alimento?
- Se eu não estiver aqui, alguém saberá explicar?
- Quem é mais vulnerável nessa situação?
“Boas práticas são construídas a partir da análise de risco real, não apenas do cumprimento formal de requisitos.”
Essas perguntas não geram multas. Mas evitam danos.
A complexidade existe e precisa ser assumida
Rotulagem é complexa e cheia de detalhes. Ingredientes compostos, traços, porções, alegações, símbolos, advertências.
Ignorar essa complexidade não a elimina. Ela apenas reaparece em forma de erro, confusão ou risco. O desafio não é simplificar demais, nem complicar mais ainda. É traduzir.
“Traduzir informação técnica é torná-la compreensível sem perder sua essência.”
O fim do arco: consciência antes da regra
Talvez o verdadeiro avanço da rotulagem, assim como de tantos outros pilares da segurança de alimentos, não esteja em criar novas exigências, mas esteja em criar mais consciência.
Quando a informação passa a ser vista como cuidado:
- ela acompanha o alimento,
- ela se adapta ao contexto,
- ela respeita quem consome.
O alimento deixa de ser apenas seguro. Ele passa a ser responsável.
Um fechamento que não fecha

Este texto não entrega respostas prontas. Ele não resolve a rotulagem. Ele não encerra o debate. Ele apenas propõe uma mudança de olhar:
“Estamos rotulando para cumprir ou para cuidar?”
Enquanto essa pergunta não fizer parte do processo, a rotulagem continuará correta no papel e insuficiente na vida real.
Prenúncio consciente da continuidade
Os próximos textos desta série caminharão do questionamento para a tradução prática: como ler um rótulo, como interpretar cada informação e como transformar exigência em escolha consciente.
Mas isso só faz sentido depois desta conversa um pouco incômoda. Porque antes de avançar sobre a rotulagem (a informação que acompanha o alimento), talvez fosse necessário refletir sobre o porquê de a escrevermos.
Leia também:
Importância da rotulagem de alimentos
5 min leituraFalar de rotulagem de alimentos costuma remeter imediatamente a listas, normas, porcentagens e exigências legais. Para muitos, é um tema técnico demais. Para outros, apenas mais uma obrigação a ser […]
Este artigo orienta compradores de matéria-prima e o time da Qualidade sobre a importância de manter vigilância mesmo sobre fornecedores de insumos já homologados. As pragas dos grãos armazenados são contaminantes com uma dinâmica própria, e pequenos descuidos resultam em enormes perdas financeiras, condenam marcas e fragilizam a responsabilidade profissional.
Imaginemos essa situação hipotética (ou nem tanto)
O Planejamento de Produção definiu a programação. O objetivo é claro: produzir 20 toneladas de um alimento cujo principal insumo é um derivado de cereais. O estoque disponível é suficiente para o lote e foi aprovado no recebimento, atendendo a todos os parâmetros de qualidade estabelecidos. Até aqui, tudo segue o manual.
Ao abrir o primeiro fardo, a equipe de produção identifica insetos vivos misturados ao insumo. O palete é imediatamente segregado e o Controle de Qualidade acionado. Desce outro palete. O problema se repete. Em poucos minutos, a constatação é inevitável: todo o estoque daquele insumo está impróprio para uso, contaminado por carunchos e/ou traças. A orientação é direta: ligue para o fornecedor.
A reposição levará quatro dias úteis. Suprimentos, Qualidade e Vendas entram em modo de crise. A produção para, o clima pesa e a diretoria é objetiva: quer um CPF na mesa. Você é designado para identificar onde aconteceu a falha e apresentar a solução. Surge, então, a pergunta clássica, dita com a convicção de quem acredita que ela resolve tudo: mas o fornecedor é homologado? Sim. Uma parceria sólida, com mais de três anos e centenas de toneladas entregues dentro das especificações.
E assim nasce um problema, em plena sexta-feira.
- Não foi erro do recebimento.
- Não houve erro na seleção do fornecedor.
- Nenhuma falha no programa de controle de pragas da indústria.
Lição aprendida: Risco biológico merece gestão de longo prazo.
Voltando aos conceitos
Insumos derivados de cereais como milho, arroz, trigo, aveia, cevada e soja, além de sementes como feijão, amendoim, grão-de-bico e girassol, são altamente suscetíveis às pragas dos grãos armazenados, como carunchos, traças e ácaros. Desde a colheita até o beneficiamento, existe um esforço contínuo para reduzir a presença desses insetos.
Outros riscos também estão presentes nessas instalações, como moscas, baratas, aranhas, roedores e pássaros. Embora importantes, esses agentes raramente resultam em contaminação direta do produto final.
O grande desafio está nos ovos dos insetos. Nunca são totalmente eliminados. Processos com bom manejo ambiental e tratamentos químicos adequados reduzem drasticamente a infestação, mas não eliminam o risco. São ovos invisíveis no envase e passam despercebidos na análise visual do recebimento. O maior risco não é o inseto visível. É o risco invisível, silencioso e perfeitamente dentro da validade. Um insumo pode cumprir a validade legal e ainda assim estar fora da condição sanitária aceitável.
Como o problema nasce (literalmente)
Semanas após o recebimento, no meio do estoque industrial, ocorre a eclosão dos ovos, e desenvolvimento do ciclo dos insetos. A velocidade desse processo varia entre espécies, mas é fortemente influenciada pelas condições ambientais, especialmente a temperatura. Acima de 30°C, a proliferação acelera.
Entre 8 e 12 semanas após a produção, um insumo contaminado já apresenta sinais claros. A infestação costuma ser percebida entre 16 e 24 semanas. Em até seis meses, o insumo pode estar completamente descaracterizado, mesmo dentro do prazo de validade.
Até alguns dias, em alguns casos, a fumigação poderia eliminar os insetos e permitir a recuperação do material após peneiramento. Mas a Nota Informativa 5/2026 ANVISA apontou com clareza inquestionável que este é um método permitido exclusivamente em instalações agrícolas (fazendas, armazenadores e portos). Era um custo relevante, mas ainda menor do que a devolução e substituição do insumo, cenário mais comum e financeiramente desgastante. Mas vale lembrar: fumigação nunca foi solução de controle; mas sim a medida de contenção quando o sistema falhou.
O fornecedor está vigilante?
Fornecedores homologados mantêm rotinas de controle de pragas, geralmente com empresas licenciadas pela ANVISA. Entretanto, poucas empresas controladoras dominam as pragas dos grãos armazenados. Controlam baratas, ratos e formigas com desenvoltura, mas não buscam conhecimento para combater pragas de grãos. Muitos profissionais sequer identificam espécies críticas (Tribolium, Sitophilus, Necrobia, Ephestia, Liposcelis etc.) ou compreendem seu comportamento.
A contenção desse tipo de contaminação passa por:
- Diagnóstico do programa controle de pragas + plano de ação (agora sem fumigação)
- Análise de riscos associados a pragas
- Treinamento contínuo do time industrial (principalmente recebimento, produção e qualidade)
É sempre mais barato investir em excelência do que arcar com devoluções ou perder credibilidade.
Expurgue o amadorismo
A indústria de alimentos brasileira cresce em volume e qualidade. Não existe espaço para improviso. Controle de pragas exige método, especialização e protocolos claros, respaldados por contratos e responsabilidades definidas. Vigilância constante de fornecedores não é exagero. É maturidade profissional.
Como já alertava John Philpot Curran: “O preço da liberdade é a eterna vigilância.”
3 min leituraEste artigo orienta compradores de matéria-prima e o time da Qualidade sobre a importância de manter vigilância mesmo sobre fornecedores de insumos já homologados. As pragas dos grãos armazenados são […]
A séria americana All her fault, bastante falada no início desse ano, trata de um assunto importante para a segurança de alimentos: a alergia alimentar.
Sem querer trazer spoilers da série, a ideia aqui é discutir a alergia à soja. Quando pensamos na soja, notamos que está presente em muitos alimentos preparados, suplementos proteicos, produtos vegetarianos (substitutos de carne) e em alimentos processados, na forma de estabilizantes ou emulsificantes, além de tofu, molho shoyu e outros.
A soja é bastante conhecida na nossa dieta principalmente pelo óleo de soja, mas pesquisas da última década, inclusive de grupos brasileiros, já demonstraram que no óleo de soja não é possível detectar quantidades da proteína alergênica da soja. Esse assunto já foi tratado em alguns artigos aqui no blog:
É preciso rotular soja como alergênico em óleo refinado?
Anvisa recua e define que óleo de soja não apresenta alérgeno
Em nome das Boas Práticas Regulatórias, Anvisa revê a decisão sobre alergênico em óleo de soja
A alergia à soja é uma reação imunológica exagerada às proteínas da soja, comum em bebês e crianças. Os sintomas podem se manifestar como reações na pele – urticária, inchaço e formigamento nos lábios; problemas digestivos como vômitos e diarreia, e alterações respiratórias como chiado e tosse. Casos graves podem causar anafilaxia, inclusive levando à morte caso não sejam controlados a tempo. Recomenda-se que a pessoa alérgica esteja sempre com epinefrina na forma de “caneta injetora”.
Os sintomas podem começar minutos ou até horas após a ingestão ou contato com a soja.
A legislação brasileira sobre alérgenos em alimentos é regida principalmente pela RDC nº 727/2022 da Anvisa, que revogou a antiga RDC 26/2015. É obrigatória a declaração da presença de principais alimentos causadores de alergias nos rótulos de alimentos embalados. A rotulagem deve destacar ingredientes alergênicos, derivados e a possibilidade de contaminação cruzada, com frases como “Alérgicos: Contém…” e a soja faz parte dessa lista de alergênicos cuja declaração é obrigatória.
Para evitar as reações alérgicas é imprescindível a leitura dos rótulos. Quando constar a soja na lista de ingredientes, ou derivados de soja, como proteína hidrolisada de soja, ou ainda a indicação de que pode conter soja, esses alimentos não devem ser consumidos pelos alérgicos.
A alimentação em restaurantes ou em outros locais com a possibilidade de reação cruzada deve ser avaliada quanto aos riscos de reação.
É importante destacar que pessoas podem ter sensibilidade diferente ao alérgeno, com reações mais brandas ou mais graves e, portanto, cada caso precisa ser avaliado e acompanhado de perto pela pessoa, família e médico.
Imagem: Polina Tankilevitch
2 min leituraA séria americana All her fault, bastante falada no início desse ano, trata de um assunto importante para a segurança de alimentos: a alergia alimentar. Sem querer trazer spoilers da […]
Muitas empresas têm indicadores, gráficos, planilha, meta mensal. Cada área acompanha o seu, cada gestor olha para o que é cobrado e, no fim, pouca gente enxerga como tudo isso se conecta com a estratégia da empresa. E quando falamos de segurança dos alimentos, estes indicadores ficam direcionados exclusivamente ao departamento de qualidade, mas não seria mais interessante se fizessem parte da estratégia do negócio? E se pudéssemos organizar as ideias para contemplar diferentes pontos de vista para a segurança dos alimentos, pensando em aprendizagem, processos, custos…?
É nesse ponto que o BSC pode auxiliar. O BSC, abreviação para Balanced Scorecard, divide os objetivos da empresa em quatro perspectivas: Finanças, Clientes, Processos Internos e Aprendizado e Crescimento. Ele serve para organizar o pensamento e ajuda a empresa a entender e programar os objetivos de forma balanceada.
Quando a gente olha para a segurança dos alimentos pelas quatro perspectivas do BSC, o raciocínio pode ficar mais claro.
O Balanced Scorecard é uma ferramenta para organização balanceada dos indicadores do negócio onde podemos incluir perspectivas de indicadores para a segurança dos alimentos.
Na perspectiva financeira, a pergunta é simples: quanto custa uma não conformidade? Todo desvio gera uma perda. Pode ser descarte, retrabalho, parada de linha ou até perda de confiança do cliente e da marca. Quando esse custo aparece nos indicadores, a segurança dos alimentos demonstra em números o resultado do negócio.
Na perspectiva de clientes, o foco é a confiança. O consumidor não conhece o processo, não vê os controles, não participa das auditorias. Ele só faz uma pergunta silenciosa: posso confiar nesse alimento? Reclamações, devoluções e percepções de qualidade dizem muito sobre essa resposta.
Já na perspectiva de processos internos, a segurança realmente acontece. É no cuidado diário, na disciplina das rotinas, no cumprimento dos procedimentos e na atenção aos detalhes. Auditorias, desvios e resultados de análise mostram se o processo está saudável ou não.
Por fim, a perspectiva de aprendizado e crescimento lembra uma coisa importante: sistema nenhum funciona sem gente preparada. Treinamento, liderança presente e ambiente de confiança sustentam todos os outros resultados.
Quando os indicadores são organizados dessa forma, a segurança dos alimentos deixa de ser um conjunto de números isolados. Ela passa a fazer parte da estratégia. E quando cada área entende como contribui para esse todo, os indicadores deixam de ser obrigação e começam, de fato, a fazer sentido.
Para concluirmos a reflexão de hoje, trago alguns insights:
Perspectiva financeira
Focada no impacto econômico das falhas ou das ações preventivas.
- Custo de não qualidade relacionado a desvios de segurança dos alimentos
- Valor de produto descartado por contaminação ou não conformidade
Perspectiva de clientes
Relacionada à confiança e à percepção do mercado.
- Número de reclamações de clientes ligadas à segurança dos alimentos
Perspectiva de processos internos
Onde a segurança realmente acontece no dia a dia.
- Percentual de conformidade em auditorias de BPF
- Número de desvios, não conformidades
Perspectiva de aprendizado e crescimento
Ligada às pessoas, treinamento e cultura.
- Percentual de colaboradores treinados em segurança dos alimentos
- Horas de treinamento em áreas críticas por colaborador
No fim das contas, o BSC só ajuda a empresa a enxergar o que muitas vezes já estava ali, porém de forma balanceada.
Gostou do conteúdo? Deixe seu comentário.
2 min leituraMuitas empresas têm indicadores, gráficos, planilha, meta mensal. Cada área acompanha o seu, cada gestor olha para o que é cobrado e, no fim, pouca gente enxerga como tudo isso […]
Os Estados Unidos vivem o maior surto de botulismo infantil registrado – o primeiro do mundo associado a fórmulas para bebês desde que essa doença foi categorizada em 1976. O que podemos aprender com este surto? Convido você, leitor, a aprofundar-se no tema por meio de três publicações — o caso pode estabelecer um novo precedente na fabricação de fórmulas infantis.
O surto resultou em uma investigação conjunta envolvendo a Administração de Alimentos e Medicamentos dos Estados Unidos (FDA) e os Centros de Controle e Prevenção de Doenças (CDC). A investigação foi realizada em parceria com o Programa de Tratamento e Prevenção do Botulismo Infantil (IBTPP) do Departamento de Saúde Pública da Califórnia (CDPH) e outros colaboradores estaduais e locais. A investigação foi relacionada à fórmula infantil ByHeart Whole Nutrition. Além disso, a empresa está colaborando com a investigação para determinar a causa raiz.
Mas qual foi a sequência temporal deste surto? Qual é o número de bebês afetados? Como foi realizado o recall? Descobriremos neste primeiro post.
Cronologia do surto, bebês afetados e recall
O primeiro alerta foi emitido pelo FDA e CDC em novembro de 2025, após um aumento nos casos de botulismo em bebês (13 casos), com a exposição à fórmula infantil sendo um fator comum. Todos os dias, novos bebês eram internados, e a Agência atualizava as informações em seu site, incluindo-as no Boletim de Alerta de Surto.
Em 19 estados (AZ, CA, ID, IL, KY, MA, ME, MI, MN, NC, NJ, OH, OR, PA, RI, TX, VA, WA, WI), 51 bebês foram impactados. Todos os 51 bebês foram internados e receberam tratamento com BabyBIG®, a antitoxina infantil. Além disso, muitos deles precisaram ser colocados em ventiladores para auxiliar na respiração. Não houve registro de mortes. Os bebês têm entre 16 e 264 dias de idade, e 22 deles (43%) são do sexo feminino. A contagem foi estendida para incluir casos de botulismo infantil registrados a partir de 24 de dezembro de 2023.
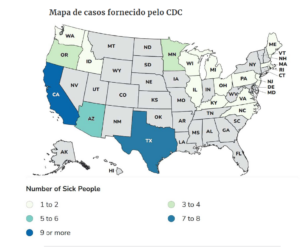
As autoridades foram informadas sobre esse conjunto de casos no dia 6 de novembro de 2025 e iniciaram a investigação. No dia 7 de novembro, recomendaram que a empresa realizasse o recolhimento voluntário de dois lotes do produto, e no dia 8 de novembro emitiram um alerta público aos consumidores. A empresa ByHeart realizou um recall voluntário, estendendo-o a todos os lotes de fórmula infantil e a todos os produtos, incluindo latas e sachês Anywhere Pack, em todo o país. Isso incluiu lojas físicas e online. A empresa ofereceu reembolso integral aos consumidores, suspendeu a produção dos alimentos e interrompeu as atividades de marketing, publicidade e parcerias com influenciadores.
O Departamento de Saúde Pública da Califórnia disponibilizou uma linha direta para ajudar cuidadores com dúvidas sobre o surto de botulismo infantil. O atendimento está disponível de segunda a sexta-feira, das 7h às 19h. Foi aconselhado aos pais e responsáveis que cessassem imediatamente o uso de fórmula infantil, que observassem os bebês que a consumiram e que procurassem assistência médica imediatamente se eles apresentassem sintomas. Ademais, foi recomendado que itens e superfícies que possam ter tido contato com a fórmula fossem higienizados com água quente e sabão ou na máquina de lavar louça. Os varejistas foram encorajados a garantir a coleta dos itens, incluindo os que foram retornados pelos clientes. Foi recomendado aos médicos que, ao suspeitar de algo, entrassem em contato imediatamente com a linha de suporte clínico do CDPH, que está à disposição 24 horas por dia, 7 dias por semana.
As empresas foram instruídas a não comercializar nem utilizar a fórmula infantil ByHeart Whole Nutrition que foi recolhida, além de lavar e higienizar itens e superfícies que possam ter entrado em contato com a fórmula recolhida. Os profissionais de saúde foram informados de que o diagnóstico inicial do botulismo infantil se fundamenta em sintomas clínicos e que devem iniciar o tratamento o mais rápido possível, sem aguardar a confirmação laboratorial. O botulismo infantil é uma doença que deve ser notificada obrigatoriamente. O departamento estadual de saúde deve ser informado sobre todos os casos suspeitos.

De acordo com informações dos consumidores da Amazon, a fórmula foi distribuída internacionalmente para 22 países. Isso inclui Argentina, Brasil, Brunei, Canadá, Chile, China, Colômbia, Equador, Egito, Hong Kong, Israel, Jamaica, Japão, Coreia do Sul, Peru, Filipinas, Romênia, Singapura, África do Sul, Tailândia e Ilhas Virgens Britânicas. Este recall internacional abrange todos os produtos ByHeart.
No Brasil, o produto era veiculado em anúncios em plataformas de comércio eletrônico. A Anvisa proibiu totalmente qualquer aspecto da fórmula infantil (comercialização, distribuição, importação, propaganda e uso). Além disso, determinou a apreensão de todos os lotes do produto em 14 de novembro de 2025 por meio da Resolução-RE nº 4.620 e emitiu a Comunicação de Risco nº 144/2025 – VISA. A medida foi motivada considerando a ausência de registro sanitário no país e o alerta do FDA.”
Em certos estados, famílias em situação de rua ou vulneráveis receberam latas doadas por meio de programas de assistência alimentar e habitacional, entre esses programas está o Departamento de Serviços Humanos do Oregon. A ByHeart informou que, desde junho de 2022, distribuiu quase 24.000 latas de fórmula, posteriormente recolhidas. E ao menos 30 famílias impactadas recorreram à Justiça, representadas pelo advogado especializado em segurança alimentar Bill Marler, que pediu ao tribunal a unificação dos casos. A ByHeart supostamente mantém 10 milhões de dólares em seguro de responsabilidade civil.
Apesar do recall internacional, quatro grandes varejistas não retiraram as fórmulas de suas prateleiras. Isso levou a FDA a emitir uma carta de advertência no dia 12 de dezembro e um comunicado à imprensa no dia 15 de dezembro, convocando os líderes da indústria alimentícia a cumprirem de forma eficaz os protocolos de recolhimento de produtos alimentícios estabelecidos pela Lei Federal.
Como acontece o botulismo infantil?
Segundo o CDC, o botulismo infantil é uma toxemia intestinal que ocorre após a ingestão de esporos da bactéria Clostridium botulinum ou de espécies associadas. Esses esporos colonizam temporariamente o intestino grosso do bebê e produzem a neurotoxina botulínica, que se liga às terminações nervosas colinérgicas e cliva proteínas intracelulares essenciais para a liberação de acetilcolina. Isso pode levar a paralisias bulbares, hipotonia e paralisia flácida simétrica e descendente. Esses esporos estão presentes naturalmente no ambiente, incluindo solo e sedimentos (poeira), e conseguem ser inseridos em ambientes de fabricação de alimentos e residenciais por meio de mãos, sapatos e outras superfícies contaminadas. Bebês podem consumir esporos de Clostridium botulinum presentes na comida ou no ambiente, tornando-os uma população vulnerável com risco de vida, enquanto crianças mais crescidas e adultos com sistemas digestivos desenvolvidos e saudáveis não são afetados.
A doença é rara, mas séria, e o diagnóstico é clínico, requerendo ação imediata, pois pode ser fatal entre bebês de 3 a 26 semanas, pois o organismo da criança, ainda em formação, não consegue combater a ação dessa bactéria tão letal. Nos EUA, é a principal causa de botulismo entre os estados. Uma das principais causas é a oferta de mel de abelha nas primeiras semanas de vida, que pode ser responsável por 5% dos casos de morte súbita em lactentes. Por isso, não se pode ofertar mel a bebês menores de 1 ano. Confira aqui um artigo anteriormente publicado neste blog sobre essa questão.
Os sintomas habituais surgem tanto de forma conjunta quanto isolada, e podem levar semanas após a ingestão do alimento. Começam com constipação, dificuldade para se alimentar (sugar e engolir), redução dos reflexos de sucção e vômito, ptose (pálpebra caída), reflexos vagarosos (ritmo diferenciado), choro fraco e alterado, expressão facial inexpressiva e falta de controle da cabeça. Isso pode progredir para problemas respiratórios e parada respiratória. Alguns pais dizem que seus bebês perderam o apetite.
No segundo post da trilogia, abordaremos a composição da fórmula infantil, os resultados das análises laboratoriais e o fabricante do produto. Até breve.
Doralice Goes é mestranda em Segurança dos Alimentos pela UFSJ, sobreviveu ao botulismo alimentar em 2022 e, desde então, dedica-se ao estudo da doença, monitora casos globais, faz palestras na indústria e é autora de livro sobre o botulismo.
5 min leituraOs Estados Unidos vivem o maior surto de botulismo infantil registrado – o primeiro do mundo associado a fórmulas para bebês desde que essa doença foi categorizada em 1976. O […]

Siga nosso conteúdo pela Newsletter
Fique sempre ligado em nossas publicações. Receba em primeira mão, direto no seu email.