Como já dizia o estatístico e professor americano William E. Deming, “o que não pode ser medido, não pode ser gerenciado”. Essa frase, aplicada no contexto de food safety, é de extrema utilidade e veracidade pois se trata de um assunto complexo em uma cadeia que movimenta bilhões de euros todos os anos e é regida por muitos atores, como produtores de alimentos, processadores, importadores e exportadores. Os políticos têm responsabilidade de estabelecer políticas governamentais e diplomáticas para fazer com que todos funcionem com harmonia e entreguem alimentos seguros tanto dentro como fora dos seus domínios. As informações e o seu gerenciamento são elementos cruciais desse universo pois estamos falando da saúde humana e animal.
O tema tem tudo a ver com o Brasil, um dos poucos celeiros do mundo atual e futuro, pois como produtor e exportador de quase tudo que se come, se bebe e se veste, é regido e influenciado por legislações e tratados internacionais que muitas vezes podem ser utilizados como verdadeiras barreiras não tarifárias e protecionistas. Resíduos de pesticidas, contaminantes do processo de produção e processamento e de produtos veterinários são e serão cada vez mais monitorados, analisados, banidos e alvos de protestos de sociedades extremamente preocupadas com o que se alimentam, muitas vezes despertando reações superestimadas e irreais por não conhecerem a seriedade e a responsabilidade para ser um agricultor/processador/exportador. Se falarmos dos países europeus, que rejeitam os GMOs e são muito conservadores e tradicionalistas, isso pode ter uma importância e impactos ainda maiores mundo afora.
Nesse caminho é que surgiram ainda nas décadas de 1970, 1980 e 1990, diretivas como as 91/414 e a 396/2005, que regulamentaram o registro, comercialização, utilização dos pesticidas na União Europeia (UE), além de definirem regras para o estabelecimento de Limites Máximos de Resíduos (LMR) harmonizados para todos. Isso levou em um dado momento à reavaliação e ao banimento de centenas de produtos considerados prejudiciais à saúde humana não somente para uso na UE, mas também para alimentos que fossem importados para dentro do bloco de países. Outras diretivas foram estabelecidas para regular os contaminantes e produtos veterinários seguindo essa mesma direção. Um texto muito interessante e que resume o exposto pode ser visto aqui.
Mas como dizia William Deming, era preciso medir e monitorar o que era resíduo ou não conformidade e o que estava dentro dos MRLs permitidos e considerados seguros para todos esses insumos, o que abarca do seu lado outra indústria não menos bilionária, a desses insumos, que também tem seus interesses e joga pesado quando se trata de banir produtos registrados, onde foram investidos muitos recursos. Como se percebe, é um jogo extremamente complexo e que vem sendo jogado há décadas. No final da linha estamos nós, os consumidores, a parte mais interessada da cadeia.
Para coordenar e harmonizar informações de tantas fontes das dezenas de países da União Europeia foi fundada em 2002 a European Food Safety Authorithy (EFSA), um organismo que visa fornecer à Comissão Europeia e à sociedade pareceres científicos independentes sobre a segurança de alimentos e os riscos possíveis nessa cadeia. Em 2021 o seu orçamento anual era de €118,6 milhões e contava com um total de 542 funcionários. A agência também apoia o Parlamento Europeu e os Estados Membros da União Europeia além de Islândia, Noruega, Suíça e Reino Unido, na tomada de decisões eficazes de gestão do risco que garantem a proteção da saúde dos consumidores e a segurança da cadeia alimentar, incluindo os alimentos para animais e aves, como as rações e vacinas.
Até então o que se tem no âmbito da UE, para integrar os dados oficiais de monitoramento da segurança de alimentos recolhidos pelos Estados-Membros e submeter à Autoridade EFSA é a plataforma Zenodo. Estes dados incluem 392 milhões de resultados analíticos derivados de mais de 15,2 milhões de amostras, abrangendo mais de 4.000 tipos diferentes de produtos alimentares compilados desde a fundação da EFSA, originados em 235 países, o que pode oferecer grandes oportunidades para a inteligência artificial analisar tendências, prever riscos e apoiar sistemas de alerta precoce, hoje existentes, mas que podem ser aprimorados haja vista a dinâmica desse imenso mercado.
Resultados
Nesse complexo cenário de muitas partes interessadas é que se apresentam os resultados do trabalho “Food safety trends across Europe: insights from the 392-million-entry CompreHensive European Food Safety (CHEFS) database”, (aqui), a ser publicado na Food Control, uma revista da European Federation of Food Science and Technology (EFFoST) e a International Union of Food Science and Technology (IUFoST), organismos já conhecidos pelos leitores desse blog e que reúnem cientistas e empresas da área de food safety na Europa e em muitos outros países.
O trabalho tem como destaques a unificação desses 392 milhões de resultados analíticos em um único conjunto de dados estruturado abrangendo pesticidas, medicamentos veterinários e contaminantes químicos em 15,2 milhões de amostras de alimentos, listando 4.035 produtos alimentícios diferentes provenientes de 235 países, ou seja, países do bloco e uma série de exportadores, incluindo obviamente o Brasil. Isso vem facilitar os problemas de acesso ao consolidar os mais de 1.000 arquivos da plataforma Zenodo com várias centenas de gigabites em um único banco de dados organizado, revelando as principais tendências no monitoramento da segurança de alimentos em toda a Europa no período 2000–2024.
Mas como foi construída essa poderosa ferramenta? De maneira resumida, o processamento concentrou-se na harmonização dos formatos de dados, na criação de identificadores exclusivos para amostras e resultados analíticos, no tratamento de valores ausentes e na remoção de duplicatas. Havia arquivos de dados separados por grupo de contaminantes, país e ano. O desenvolvimento do banco de dados seguiu um processo estruturado começando com o download e a extração automáticos dos arquivos de dados brutos da EFSA, resumido na Figura 1.
Figura 1. Esquema da elaboração do banco de dados nas diferentes fases e suas aplicações.
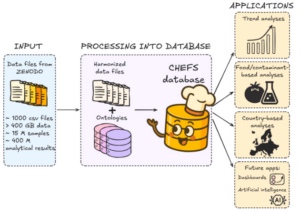
A próxima etapa envolveu a análise e harmonização dos diferentes formatos de dados, não apenas entre os principais grupos de contaminantes (pesticidas, contaminantes químicos e resíduos de medicamentos veterinários), mas também dentro deles. Para permitir uma integração de dados eficiente e repetível foram desenvolvidos scripts para o processamento automatizado dos arquivos de dados brutos da EFSA e sua importação para o banco de dados CHEFS. Um resumo é apresentado na Tabela 1.
Tabela 1. Número e percentagem de resultados analíticos na base de dados CHEFS. Os resultados analíticos com os códigos de avaliação “Superior às Quantidades Máximas Permitidas”, “Não Conforme”, “Detectado” e “Insatisfatório” foram definidos como acima dos limites ou “não conformes”.
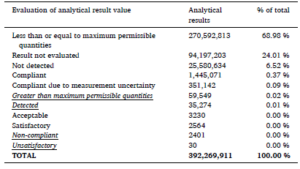
Um total de 4.170 IDs de contaminantes foram incluídos no conjunto de dados CHEFS abrangendo as categorias “contaminantes químicos”, por exemplo, metais pesados, micotoxinas, dioxinas, “resíduos de pesticidas” e “resíduos de medicamentos veterinários” aqui chamado de VMPR. Foram examinadas as tendências nos perigos mais frequentemente testados, agregando todos os resultados analíticos associados a cada ID de contaminante exclusivo em todos os países, anos e tipos de produto por tipo de contaminante. Os 10 contaminantes mais frequentemente analisados foram visualizados usando gráficos de barras, estratificados pelas categorias acima mencionadas. Foram realizadas análises estatísticas descritivas para três tipos principais de análises: tendências ao longo dos anos, estatísticas de contaminantes e alimentos e estatísticas por país. Por questões de espaço vou me limitar a análise dos resultados das tendências ao longo dos anos e estatísticas de contaminantes, dando um foco maior aos resíduos de pesticidas, área da minha especialidade, deixando as estatísticas por país para uma outra oportunidade.
Resultados: tendências ao longo dos anos
O número de resultados analíticos para contaminantes químicos, resíduos de pesticidas e VMPR apresentou um aumento geral ao longo do tempo (Figura 2). Foram considerados dados de monitoramento posteriores a 2000, embora os dados disponíveis na EFSA comecem em 1970. Enquanto os resultados analíticos de contaminantes químicos são registrados desde 2.000 no banco de dados da EFSA, os dados de monitoramento de resíduos de pesticidas só estavam disponíveis após 2010 e os de VMPR somente após 2016.
Figura 2. Número de resultados analíticos e número de resultados analíticos acima dos limites legais de (a) contaminantes químicos, (b) resíduos de pesticidas e (c) VMPR.
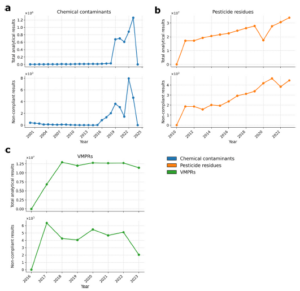
Os resultados mostrados nos gráficos são claros. Todos os grupos mostram um aumento ao longo do tempo no número de resultados analíticos, e os resíduos de pesticidas mostram um aumento ao longo do tempo no número de resultados analíticos acima do limite (non compliance) de maneira consistente a partir de 2011. Isso se deve a vários fatores, incluindo o refinamento das técnicas para coleta e detecção de resíduos desde o início da série em 2010.
Apesar do avanço nas técnicas de produção e no aumento na produção de alimentos mais saudáveis, como os orgânicos, uso de produtos biológicos, adoção de protocolos de garantia da qualidade como o Global GAP, Rain Forest, SGS, HACCP etc., a pressão na produção da agricultura tradicional e seus desafios de aumento da produtividade são cada vez mais impactados por fatores externos como o aquecimento global, que diminui o ciclo de reprodução de pragas e doenças e leva ao aumento no uso de pesticidas, bem como o aumento da resistência a esses produtos devido ao uso continuado e muitas vezes sem critérios, seja por desconhecimento dos efeitos ou pela necessidade, que não é justificada. Os resultados estão aí expostos.
Estatísticas baseadas em contaminantes
Ao analisar as estatísticas baseadas em contaminantes, é importante observar que, dos 4.529 IDs de contaminantes no conjunto de dados, apenas 3.180 eram únicos. Isso ocorre porque alguns IDs de contaminantes estavam associados a vários tipos de resultados analíticos e, portanto, não eram exclusivos de um único tipo de resultado: 2,3% (n = 73) dos IDs de contaminantes únicos estavam incluídos em todas as três categorias de perigo (ou seja, contaminantes químicos, resíduos de pesticidas e VMPR), o que significa o pior dos mundos para os consumidores. E 37,8% deles foram usados por duas das três categorias. Resíduos de pesticidas e VMPR apresentaram a maior sobreposição.
Os 10 principais contaminantes mais analisados por categoria são mostrados na Figura 3. Entre os contaminantes químicos, o chumbo (Pb) foi o contaminante mais testado, com 133.264 resultados analíticos (3,1% do total de 4.344.679 resultados analíticos para 897 contaminantes únicos no grupo de contaminantes químicos), seguido por cádmio (Cd) (2,9%) e aflatoxina B1 (1,8%).
Para 1.612 resíduos de pesticidas, os três principais contaminantes foram clorpirifós com 949.017 resultados analíticos (0,31%), diazinon 944.958 (0,31%) e pirimifós-metil 935.180 (0,30%). Ao analisar em detalhe essas informações vemos que a maioria dos produtos são organofosforados (clorpirifós, diazinon, pirimifós-metil, methidation, triazopós, profenofós), um dos grupos químicos de inseticidas mais antigos usados na agricultura e que vêm sendo utilizados há mais de 60 anos, cujos registros para uso na Europa e para importação pelo bloco em grande parte foram banidos já há algum tempo. No Brasil poucos produtos ainda restam e em alguns casos são registrados para uso emergencial (exemplo: dimetoato para cultura dos citros), haja vista que opções mais interessantes do pronto de vista de eficácia e toxidade estão disponíveis aos agricultores, mas seus resíduos persistem mostrando que ainda são utilizados de maneira significativa. A tendência é que diminuam ao longo dos próximos anos, mas a distância entre um produto ser banido, descontinuado e seu uso ser totalmente finalizado é grande, até porque as legislações preveem um tempo para que isso ocorra.
Temos que também levar em conta que centenas de países exportam para a EU, entre eles países “em desenvolvimento” onde a utilização desse tipo de produtos não sofre o mesmo controle de países “desenvolvidos” e têm diferentes desafios no campo da produção e processamento. Isso também se passa com os piretróides (deltametrina e bifentrina), segunda categoria em ocorrência, que são pesticidas que ainda continuam a ser utilizados em larga escala, muito eficazes e apresentam na sua maioria um baixo custo, Não existe previsão que seu uso seja descontinuado, ou seja, seus resíduos continuarão a aparecer de modo consistente. Quanto à azoxystrobina, único fungicida listado, por ser um produto muito utilizado para frutas e hortaliças, na produção e na pós-colheita, também haverá sempre registro de seu resíduo, bem como o uso de produtos do seu grupo, as estrobilurinas.
O contaminante dentro da categoria VMPR com o maior número de resultados analíticos foi a doxiciclina com 2.877.150 resultados analíticos (3,54%), seguida pela eritromicina com 2.838.678 (3,49%) e danofloxacina 2.834.309 (3,48%) (Fig. 3).
Figura 3. Os 10 principais contaminantes mais analisados para cada grupo de risco: a) contaminantes químicos, b) resíduos de pesticidas e c) VMPR, agregados em todos os países e anos. As porcentagens que ultrapassam os limites legais são mostradas nos gráficos de barras à direita.

Conclusões
Esse é um tema sobre o qual poderíamos escrever infinitas páginas devido à sua abrangência e complexidade. O mais importante, a meu ver, é o que pode ser feito com base nesses resultados. Apesar de despertar reações apaixonadas e muitas vezes até irracionais de todos os lados dessa mais que complexa cadeia, ninguém quer, como consumidor, ter à sua mesa alimentos com alto risco de contaminação. Certamente existem nesse momento muitas pessoas, instituições como a própria EFSA, governos da UE e todos aqueles que alimentam esse imenso mercado, desenvolvendo e aprimorando meios, políticas e ferramentas para que essas curvas que apontam aumentos nas contaminações diminuam. Temos que concordar que não é uma missão fácil, mas sistemas como o CHEFS trarão uma contribuição imensa a todo esse processo a partir do momento em que expõem os pontos mais críticos e urgentes para propor mudanças.
Marcos Pozzan é engenheiro agrônomo pela ESALQ/USP, atuando há 35 anos no agribusiness nas áreas de consultoria, segurança de produtos e certificações Global GAP, Rainforest, IFOAM. É MSc pela Universidade Politécnica de Valencia, Espanha. Atualmente vive em Portugal acompanhando tendências em food safety na Europa
9 min leituraComo já dizia o estatístico e professor americano William E. Deming, “o que não pode ser medido, não pode ser gerenciado”. Essa frase, aplicada no contexto de food safety, é […]





 Carina (foto) tem graduações em Tecnologia de alimentos e em Nutrição e atualmente é doutoranda do programa de Ciência de Alimentos da Universidade Estadual de Londrina. O blog conversou com ela para saber mais detalhes deste projeto.
Carina (foto) tem graduações em Tecnologia de alimentos e em Nutrição e atualmente é doutoranda do programa de Ciência de Alimentos da Universidade Estadual de Londrina. O blog conversou com ela para saber mais detalhes deste projeto. O manual traz informações práticas para todas as etapas da manipulação de alimentos, incluindo higiene pessoal e da cozinha, escolha, higienização e armazenamento dos alimentos, preparo e pós-preparo, prevenção da contaminação cruzada, uso de detergentes, manejo do lixo doméstico, leitura de rótulos e verificação da validade dos alimentos.
O manual traz informações práticas para todas as etapas da manipulação de alimentos, incluindo higiene pessoal e da cozinha, escolha, higienização e armazenamento dos alimentos, preparo e pós-preparo, prevenção da contaminação cruzada, uso de detergentes, manejo do lixo doméstico, leitura de rótulos e verificação da validade dos alimentos.