6 min leituraEm um mundo cada dia mais globalizado, em que cadeias de suprimentos estão conectadas e que despesas logísticas representam uma grande fatia dos custos finais dos alimentos, os gestores da qualidade e os profissionais de Food Safety precisam tomar decisões rápidas e sempre com muita segurança. Quando o assunto é detecção de patógenos, mais que apenas uma questão “de negócios”, a assertividade e a rapidez na entrega do resultado são essenciais para a segurança e a saúde do consumidor.
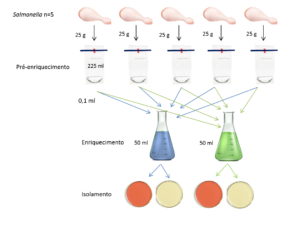
Entretanto, os métodos clássicos de microbiologia e suas técnicas, apesar de sua singularidade e confiabilidade, são compostos por inúmeras etapas que demandam muitos dias até que seja possível obter um resultado confirmado1. Para detecção de Salmonella, por exemplo, um dos principais patógenos de preocupação da indústria, utilizando o método tradicional ISO 6579:2017, a liberação de uma análise apenas será realizada entre 5 e 7 dias2.
Nesse sentido, os métodos rápidos alternativos surgiram como uma contraposição aos métodos tradicionais, com a finalidade de trazer rapidez para o diagnóstico de micro-organismos patogênicos. Hoje, existem diferentes metodologias fundamentadas em métodos moleculares, imunológicos ou até mesmo técnicas de cultivo aprimoradas, que oferecem não só redução de tempo, mas trazem facilidade e tornam o laboratório de microbiologia mais otimizado3.
Porém, algumas dúvidas ainda pairam na cabeça de muitos microbiologistas no momento de mudar de uma metodologia tradicional para uma alternativa: afinal, métodos alternativos rápidos podem ser aplicados para qualquer análise e em qualquer indústria de alimentos? O que a legislação e órgãos reguladores falam sobre isso? Como escolher uma metodologia e como é feita a implementação correta desses métodos na rotina?
O que dizem as normativas
Para responder a essas e a outras questões, o primeiro passo é entender a atuação dos dois principais órgãos reguladores em alimentos: MAPA (Ministério da Agricultura, Pecuária e Abastecimento) e ANVISA (Agência Nacional de Vigilância Sanitária – ligada ao Ministério da Saúde), e o que eles dizem sobre o monitoramento microbiológico.
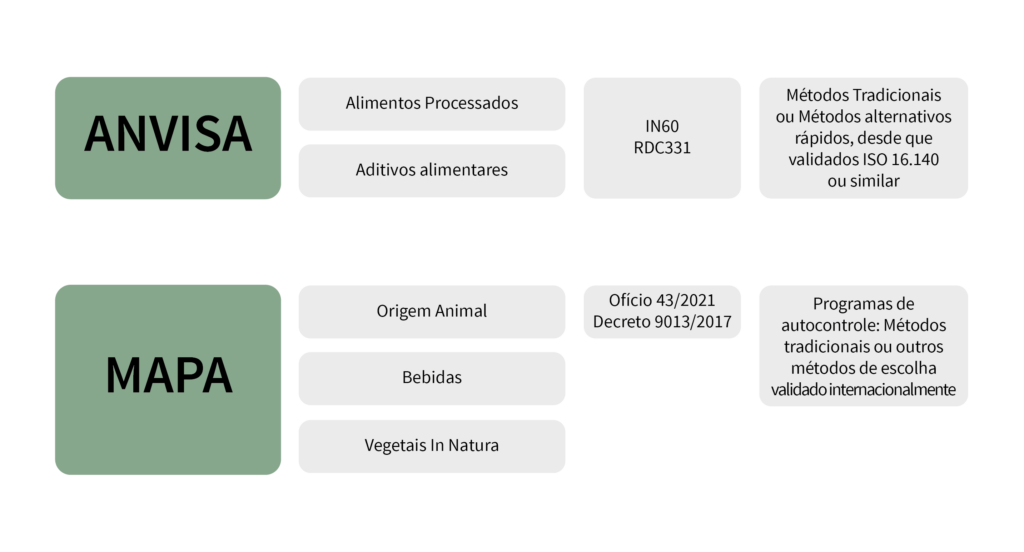
De maneira resumida, a ANVISA atua em toda a cadeia produtiva de alimentos e, por meio da RDC 331 e da IN 60, ambas de 2020, estabelece e monitora padrões microbiológicos em produtos prontos para o consumidor – de origem animal ou não. Segundo este órgão, para o monitoramento microbiológico (não só de patógenos, mas também de deteriorantes) permite-se às indústrias a utilização de métodos alternativos em todas as análises, desde que eles demonstrem, ao menos, equivalência analítica em relação aos métodos tradicionais, comprovadas por meio de estudo de validação ISO 16.140-2 ou outra de reconhecimento internacional4,5.
Já o MAPA – cujas competências incluem a fiscalização de produtos exclusivamente de origem animal, bebidas em geral e vegetais in natura – de forma um pouco mais restrita, concede autorização apenas para a aplicação de métodos reconhecidos e realizados por laboratórios credenciados quando se trata de análises oficiais. Entretanto, recentemente o órgão emitiu, através do Ofício Circular n°436, documento afirmando que as indústrias devem realizar monitoramento da qualidade de todo o seu processo produtivo, matérias-primas e produtos de origem animal, através de “programas de autocontrole”, fazendo uso de métodos com reconhecimento técnico e científico comprovados, e garantindo evidências auditáveis que comprovem a realização dos ensaios e efetividade do monitoramento. Em outras palavras, isso quer dizer que na visão do MAPA, para as análises internas, de controle, é permitido usar métodos rápidos reconhecidos internacionalmente.
Como escolher o método
Seja para a ANVISA ou para o MAPA, quaisquer métodos utilizados devem possuir comprovação técnica. Isso quer dizer que, independentemente do fabricante ou do tipo de teste, o método escolhido deve obrigatoriamente ter sido submetido a um amplo estudo de validação, preferencialmente interlaboratorial, conduzido por uma entidade terceira, que comprove o desempenho do método em questão em relação ao de referência. Existem diferentes protocolos para esse tipo de estudo de validação, os quais incluem os estabelecidos por organizações como BAM/FDA (Bacterial Analytical Manual/U.S Food & Drug Administration), AOAC (Association of Official Analytical Chemists) e o mais usual no Brasil, a ISO (International Organization for Standardization). Importante pontuar que todo esse (trabalhoso) processo é feito pelo próprio fabricante ou proponente do método e, excetuando os casos em que ocorra uma mudança essencial, só é realizado uma única vez7.
Uma dica valiosa é solicitar esses relatórios aos fabricantes e ir a fundo nas leituras. Esses documentos trazem informações importantíssimas como sensibilidade, robustez e especificidade do método. Retomando o exemplo da detecção de Salmonella e levando em consideração que esse gênero é composto por mais de 2.500 sorotipos diferentes8, em casos em que haja a necessidade de detectar um sorovar específico, por exemplo, faz-se necessário confirmar se, de fato, ele foi incluído na validação e se o método é capaz de recuperá-lo.
Portanto, desde que a metodologia escolhida atenda a essas premissas, os demais critérios são facilidade de utilização, custo-benefício, tempo de resposta e compatibilidade entre a estrutura física e de pessoal do laboratório com o método.
Como implementar o método
Na contramão do que muitos acreditam, ao laboratório que escolher utilizar algum tipo de metodologia analítica alternativa, seja ela baseada em kits comerciais prontos ou não, cabe apenas a realização de uma “verificação de implementação”. Isso não passa de uma simples bateria de testes para atestar que o desempenho do método aplicado à rotina e executado pela equipe de cada um dos laboratórios é equivalente àquela encontrada no estudo oficial de validação.
Os procedimentos detalhados deste tipo de verificação normalmente são descritos nas próprias normas ou manuais da BAM, AOAC, dentre outros. Na parte 3 da série ISO 16140:2014, por exemplo, são detalhados diversos tipos de protocolos que podem ser aplicados para essa finalidade. Em alguns casos, a simples realização de sete replicatas de amostras com concentração de contaminação conhecida já é suficiente para avaliar (e eventualmente atestar) a correta implementação do método alternativo rápido9.
Portanto, para quem se preocupa com a Segurança de Alimentos, a detecção de micro-organismos patogênicos, apesar de ser tarefa praticamente ininterrupta, não precisa ser árdua. Nesse sentido, a Neogen apresenta o método OBOP – One Broth, One Plate, uma solução rápida e segura, com possibilidade de resultados confirmados em 48 horas.
OBOP Salmonella e OBOP Listeria
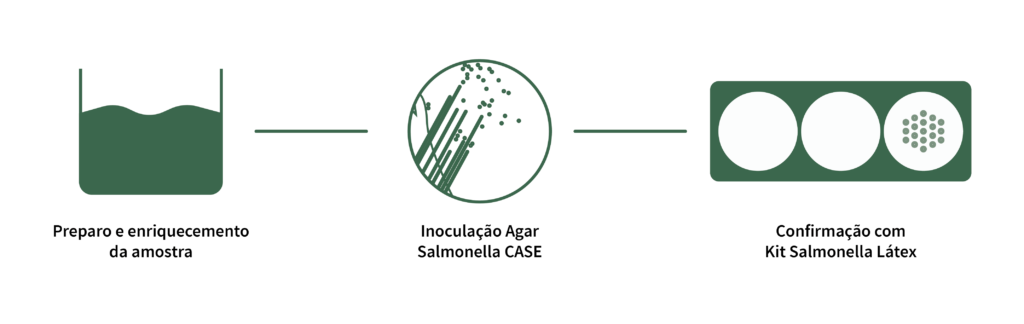
Com aprovação ISO 16140 e AOAC e com performance superior aos métodos de referência, as duas opções de testes OBOP oferecem um fluxo de trabalho simples, baseado em microbiologia tradicional de cultivo e que não necessita de equipamentos especiais. São apenas duas etapas de teste: um enriquecimento altamente seletivo e exclusivo Neogen, e um plaqueamento em meio cromogênio com diferenciação superior das colônias.
- Maior especificidade e sensibilidade: Testes mais sensíveis que a ISO 6579 e ISO 11290.
- Desempenho aprimorado com cepas atípicas: Recuperação de salmonelas imóveis como S. Pullorum e S. Gallinarum, cepas monofásicas, lactose positivas e com atividade fraca de esterase.
- Confirmação flexível: diferentes opções validadas para confirmação das colônias características, incluindo teste de apenas 10 minutos. Consulte um representante Neogen para saber mais!

Lauane Gonçalves
Especialista em Microbiologia Neogen
Referências
1. RAJAPAKSHA P., Elbourne A., Gangadoo S., Brown R., Cozzolino D., Chapman J. A review of methods for the detection of pathogenic microorganisms. Analyst. (2019). 14,144(2),396-411. doi: 10.1039/c8an01488d. PMID: 30468217.
2. BRASIL, Ministério da Saúde. Secretaria de Vigilância em Saúde. Boletim Epidemiológico. Brasília, 2019.
3. RIPOLLES-AVILA C, Martínez-Garcia M, Capellas M, Yuste J, Fung DYC, Rodríguez-Jerez J-J. From hazard analysis to risk control using rapid methods in microbiology: A practical approach for the food industry. Compr RevFood Sci Food Saf. 2020;1–31. https://doi.org/10.1111/1541-4337.12592
4. BRASIL, Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Instrução normativa n°. 60, de 23 de dezembro de 2019.
5. BRASIL, Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução de Diretoria Colegiada n°. 331, de 23 de dezembro de 2019.
6. BRASIL, Ministério da Agricultura, Pecuária e Abastecimento. Secretaria de Defesa Agropecuária. Departamento de Inspeção de produtos de Origem Animal. Ofício Circular n°. 43, de 11 de agosto de 2021.
7. INTERNATIONAL ORGANIZATION FOR STANDARDIZATION. ISO 16140-2:2016. Microbiology of the food chain — Method validation — Part 2: Protocol for the validation of alternative (proprietary) methods against a reference method.
8. ELNEKAVE E., Hong S. L., Lim S., Johnson T. J., Perez A., Alvarez J. (2020). Comparing Serotyping With Whole-Genome Sequencing for Subtyping of Non-Typhoidal Salmonella Enterica: A Large-Scale Analysis of 37 Serotypes With a Public Health Impact in the USA. Microb. Genom. 6, mgen000425. doi: 1099/mgen.0.000425
9. INTERNATIONAL ORGANIZATION FOR STANDARDIZATION. ISO 16140-3:2021. Microbiology of the food chain — Method validation — Part 3: Protocol for the verification of reference methods and validated alternative methods in a single laborator
6 min leituraEm um mundo cada dia mais globalizado, em que cadeias de suprimentos estão conectadas e que despesas logísticas representam uma grande fatia dos custos finais dos alimentos, os gestores da […]