Já expliquei no post Por que confiar cegamente em análises microbiológicas de produto acabado pode ser uma furada que estatisticamente é bem difícil detectar um defeito em produto acabado analisando um pequeno número de amostras. E mesmo quando o número de amostras é aumentado, ainda há um importante risco de aprovação de um lote que apresente contaminação. É por isso que deve haver cautela na interpretação de resultados de análises microbiológicas dos lotes compostos.
Análises microbiológicas geralmente são feitas por lote (ou lotes compostos) e os resultados devem ser interpretados com cuidado uma vez que se considera que o lote é a representação de uma condição padronizada que é muito mais teórica do que prática.
Vamos à definição de lote segundo a ICMSF:
Lote é o total de unidades de um produto produzido, manuseado ou armazenado em condições idênticas, dentro de um determinado período.
Do lote, se retira uma amostra/unidade amostral, que segundo a RDC 12/01, 3.7:
Porção ou embalagem individual que se analisará, tomado de forma totalmente aleatória de uma partida como parte da amostra geral.
Não existe legislação no Brasil que determine como o lote deve ser definido na fabricação de alimentos. Assim, fica a cargo do fabricante fazê-lo. Na prática, costuma ser determinado por um destes caminhos: 1) Pela receita/formulação, onde uma batelada recebe um código atribuído a uma mistura de ingredientes que deu origem ao todo 2) Por tempo. Intervalos de tempo como um turno ou um dia de fabricação determinam esta condição que delimitam o lote.
Variabilidade de resultados em um mesmo lote
Gostaria de abrir os olhos para um fator de variabilidade adicional na interpretação de resultados microbiológicos: o lote. Por questões práticas, ele não é tão homogêneo como as definições preconizam.
Imagine a situação em que um lote é definido por tempo, que seja um turno. Ao longo deste turno, várias bateladas ou receitas são pesadas por um operador de formulação. Porém, durante o turno vão acabando as matérias primas de um mesmo lote mãe e são abertas novas embalagens que podem até ser de um fornecedor diferente do que o que foi pesado há duas horas. Não estamos mais falando de um lote de condições idênticas. As matérias-primas mudaram!

No segundo caso, o de um lote atribuído por formulação, vamos supor que a mesma receita percorra trechos diferentes de uma linha de produção. Vamos a um caso fictício em que a causa da contaminação possa ser uma das mangueiras da recheadora ou a canaleta com um ponto de difícil limpeza por onde está passando a manteiga, como ilustrado abaixo. Pronto, esse lote também não está homogêneo! Imagine se for retirada uma amostra de um lado só da linha para análise.

A causa da contaminação se refletirá no resultado microbiológico da análise
Num exercício fictício imagine 3 causas possíveis para a contaminação de uma peça de carne assada pronta para consumo:
- A carne foi contaminada pós cocção pelas mãos do manipulador ou alguma superfície do processo (bandeja ou esteira transportadora. A contaminação vai se apresentar espalhada pela superfície onde houve o contato.
- A contaminação se deu por causa de um fatiador e os microrganismos se distribuirão ao longo da face cortada, sendo mais concentrada no início.
- A cocção foi insuficiente, tendo sobrevivido patógenos no centro do produto.
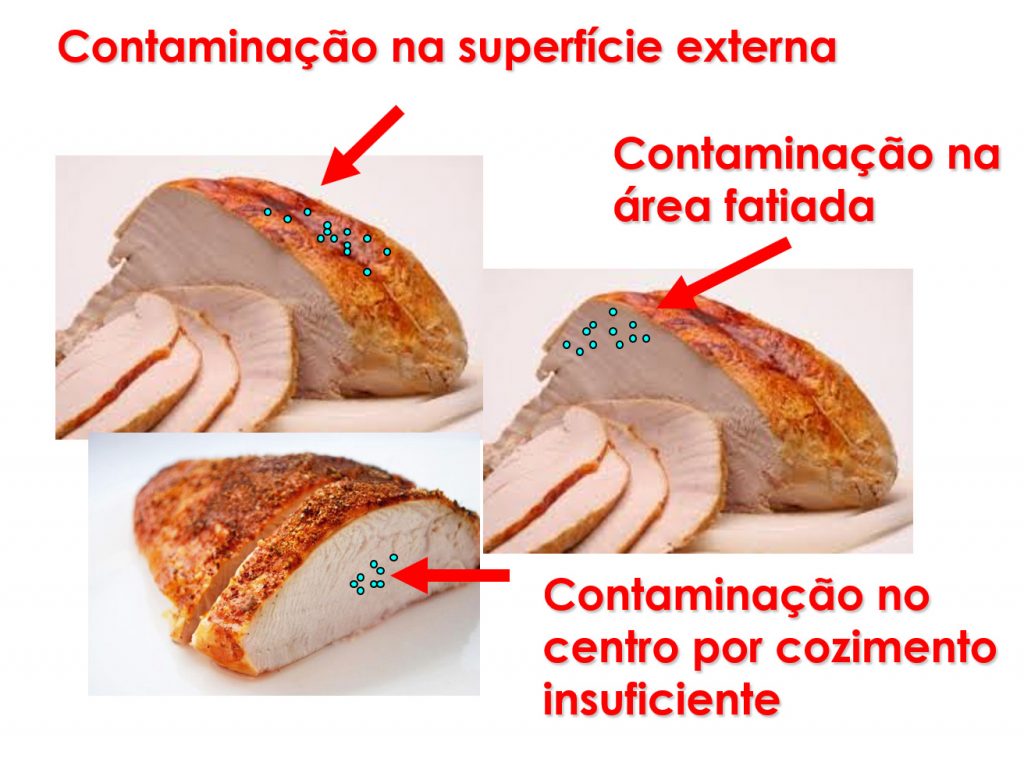
Você consegue imaginar que a forma de tomada de amostra das peças desta carne pode contribuir para se encontrar ou não o contaminante e que este pode passar não detectável? Note que não é tão fácil assim ser “sorteado” e “tirar a sorte grande” de conseguir detectar o problema antes de chegar ao consumidor.
Amostragem de lote composto – quem está se enganando?
Agora vamos a uma situação observada em algumas empresas: a adoção de lotes compostos, ou “pool” de amostras, que fazem “render” os resultados. Se você não conhece, funciona assim: um fabricante produziu 10 lotes de um determinado produto, e para economizar em análises, ao invés de tomar uma amostra de cada um e realizar 10 análises, vai tomar uma amostra de cada lote, homogeneizá-las e realizar uma análise só. Não é uma ideia brilhante?

Lamento informar que com essa “técnica” a capacidade de detecção do patógeno foi reduzida em 90%! E sem contar que, se foi retirada uma única amostra do lote, por mais aleatória e bem-feita que seja, já não estamos falando de plano de amostragem representativo.
Esta situação parece ser muito econômica e funcionar bem até que…saia um positivo!!!
No caso do lote composto, como é que vamos rastrear a causa-raiz do problema? Qual dos dez lotes está comprometido? Qual o tamanho do bloqueio de lote ou recolhimento a ser feito? Está pensando agora em “compensar” a situação analisando os lotes em separados e caso não saia positivo, era só um susto?
Aguarde o post “Tive um positivo para Salmonela. Repito a análise e se der negativo, tudo bem?” para tratarmos desta questão!
Leia também:
https://foodsafetybrazil.org/analise-microbiologica-de-alimentos-importancia-do-plano-de-amostragem/


Angelina
Existe alguma legislação que fale sobre a frequencia dessas análises?
Juliane Dias
Olá Angelina, Não há frequência estabelecida por lei. O seu produto deve cumprir a qualquer momento com as especificações e cabe a empresa, com base em métodos técnicos e científicos adequados, determinar esta periodicidade. Juliane
Maria Juliana
Extremamente esclarecedor! Obrigada por compartilhar seu conhecimento!
Juliane Dias
Que bom, Ju! Aplique na prática. Bj.
Carlos
Oi Juliane bom dia…
Não consigo cadastrar meu e-mail, o sistema só aceita terminação com .br Meu email termina com .com…
Da uma olhada pra nós… Obg
Talita Rosa Mansur
Oi Juliane !
Adorei o post.
Vivi isso na prática e sinto muita dificuldade em explicar isso para o pessoal da área.
Trabalhei por um tempo com positive release de caminhão de matéria prima. O caminhão só poderia descarregar depois da análise de micro.
Imagina o que é uma amostra de 25g em um caminhão de 30.000 litros?
Dor de cabeça na certa! Vira e mexe tinhamos problema dentro da fábrica.
Espero que mais pessoas se conscientizem de que temos que garantir todos os programas de pré -requisitos, pois a análise microbiológica pode ser como procurar uma agulha no palheiro.
Pingback:
Everton Santos
Parabéns, estou adorando o tema do assunto! Muitas empresas usam esse método Pool, e muitas delas liberam o lote quando após um resultado positivo é obtido um resultado negativo na segunda análise. Vai que a “sorte” de pegar a contaminação foi só na primeira vez … Nem para fazer um “Melhor de três” antes de liberar!
Everton Santos
Já vi casos também que o equipamento é amostrado, o resultado é positivo e a maior atenção é em higienizar o equipamento e fazer uma nova amostragem para ter um registro de conformidade do que se preocupar com o produto que foi produzido nessas condições …
Juliane Dias
Essa foi uma das motivações para escrever este post! E ainda valeria um tópico específico para equipamentos, Everton!
Rodrigo Alves Pereira
Boa tarde Juliane.
Tenho dificuldade em explicar a variação de resultados microbiológicos para o restante da equipe. Por exemplo: para aeróbios mesófilos temos resultados de 1.000 a 160.000 UFC/g, a equipe insiste em repetir análises até atingir o resultado esperado, o que entendo ser errado, gostaria de saber se há intenção em criar um post sobre essa interpretação de resultados para os não especializados nesse assunto.
Obrigado.