Um recall por leite não declarado em snacks mostra como um desvio aparentemente banal de mix de produto pode escalar rapidamente para risco regulatório, reputacional e de segurança dos alimentos. O caso reforça que gestão de alergênicos depende tanto de processo quanto de disciplina operacional.
A Frito-Lay anunciou o recall de lotes específicos de Miss Vickie’s Spicy Dill Pickle Potato Chips porque algumas embalagens poderiam conter chips sabor jalapeño e, com isso, leite não declarado. Segundo o FDA, os produtos podem ter sido distribuídos a partir de 15 de janeiro de 2026 em seis estados norte-americanos: Arkansas, Louisiana, Mississippi, Novo México, Oklahoma e Texas. A empresa informou que identificou o problema após contato de consumidor e que, até a publicação do alerta, não havia relatos de reações alérgicas associados ao caso.
O que este recall realmente mostra
À primeira vista, trata-se de um incidente simples: um produto entrou em embalagem errada. Mas esse tipo de ocorrência expõe uma fragilidade recorrente na indústria de alimentos: a ideia de que o controle de alergênicos se resume à formulação ou à declaração de ingredientes.
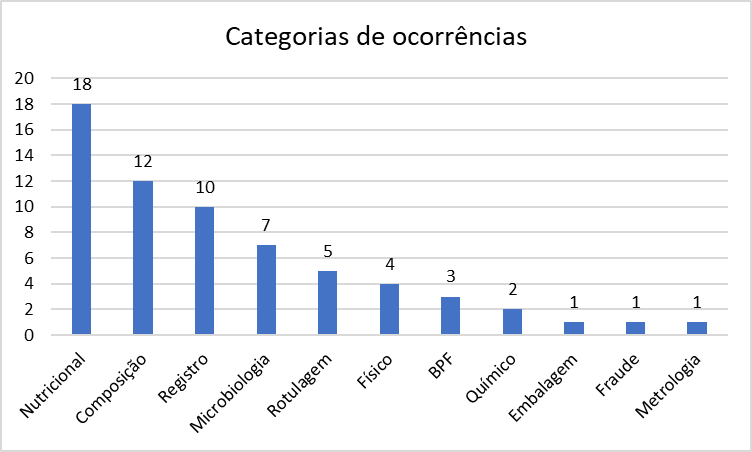
Na prática, recalls por alergênicos costumam nascer em pontos muito operacionais da rotina fabril e logística: troca de produto, liberação de linha, conferência de material de embalagem, segregação física, revisão de códigos e reconciliação entre o que foi produzido e o que foi rotulado. O próprio histórico técnico reunido pelo Food Safety Brazil mostra que erros de rotulagem seguem entre as causas mais comuns de recalls ligados a alergênicos.
Quando o risco não está no alimento “errado”, mas na informação errada
Para a maioria dos consumidores, o produto envolvido no recall pode não representar risco. No caso específico comunicado pela Frito-Lay, o problema é crítico para pessoas com alergia ao leite ou sensibilidade severa, que podem sofrer reação grave ou potencialmente fatal ao consumir um alimento cuja rotulagem não sinaliza esse perigo.
Esse ponto merece atenção porque, em alergênicos, a segurança não depende apenas da ausência do agente. Ela depende também de informação correta, clara e confiável. Quando a embalagem afirma uma identidade e o conteúdo real é outro, há falha simultânea de segurança, conformidade e comunicação de risco.
O erro parece pequeno, mas a consequência é grande
Mistura de sabores, troca de embalagens e falhas de identificação costumam ser tratados internamente como desvios de rotina. O problema é que, diante de um alergênico não declarado, esse desvio muda de categoria. Ele deixa de ser apenas perda operacional e passa a ser evento com potencial de:
- recall;
- exposição do consumidor vulnerável;
- acionamento regulatório;
- dano reputacional;
- retrabalho em rastreabilidade e investigação.
O que a indústria deveria revisar depois de um caso como esse
O caso da Frito-Lay é um lembrete útil de que programas de alergênicos falham menos por desconhecimento conceitual e mais por quebra de execução. Em especial, recomenda-se revisar cinco pontos:
1. Controle de troca de produto
Sempre que há mudança entre SKUs visualmente parecidos, o risco de mistura aumenta. Isso vale ainda mais para linhas com alta cadência e baixa janela para conferência.
2. Liberação de linha com foco em identidade
A pergunta crítica não é apenas “a linha está limpa?”, mas também “o produto certo está na embalagem certa?”. Esse segundo bloco de verificação nem sempre recebe o mesmo rigor.
3. Gestão física de embalagens e rótulos
O Food Safety Brazil já destacou que uma das maiores causas de recall por alergênicos está no uso incorreto de rótulos e na gestão inadequada desses materiais no ambiente fabril. Separação física, controle de entrada na linha e reconciliação de sobras continuam sendo controles básicos, mas indispensáveis.
4. Resposta rápida a desvios vindos do mercado
Segundo o FDA, o problema foi identificado após contato de consumidor. Isso reforça a importância de canais ativos de complaint handling e de investigação rápida de desvios aparentemente isolados.
5. Critério de risco para alergênicos
Nem todo desvio de embalagem gera o mesmo impacto. Quando há potencial presença de alérgeno não declarado, a avaliação deve ser imediata, conservadora e multidisciplinar, envolvendo qualidade, assuntos regulatórios, operações e gestão de crise.
Aplicação prática para indústria, qualidade e regulatório
Para profissionais de qualidade, este caso é útil porque mostra que gestão de alergênicos é também gestão de interface: produção com embalagem, PCP com expedição, qualidade com SAC, regulatório com rotulagem.
Na indústria, a aplicação prática é objetiva:
- revisar análise de perigos para incluir cenários de troca de produto e embalagem;
- reforçar validação e verificação de line clearance;
- limitar materiais de embalagem disponíveis simultaneamente na linha;
- usar dupla checagem em trocas críticas;
- testar rastreabilidade e tempos de reação para recalls por rotulagem;
- tratar desvios de identidade de produto como potencial evento de segurança, e não apenas de eficiência.
Para regulatório, o aprendizado é igualmente claro: a conformidade do rótulo não termina na aprovação de arte. Ela depende de execução correta até o produto chegar ao mercado.
Resumindo:
- Impacto: um erro operacional simples pode se transformar em recall amplo quando envolve alergênico não declarado.
- Recomendação prática: revisar controles de troca de produto, gestão física de embalagens e verificação de identidade na liberação de linha.
- O que monitorar: incidentes de rotulagem, reclamações de consumidores e tendências de recalls por alergênicos não declarados.
3 min leituraUm recall por leite não declarado em snacks mostra como um desvio aparentemente banal de mix de produto pode escalar rapidamente para risco regulatório, reputacional e de segurança dos alimentos. […]