O ácido hipocloroso é um novo e promissor ativo desinfetante com apelo sustentável, porque é obtido pela eletrólise de água e sal e não tem efeitos nocivos ao meio ambiente. Esse ativo é encontrado na água eletrolisada e sua concentração varia em função do pH.
O processo de eletrólise de água e sal para a produção de água eletrolisada como agente bactericida começou em 1987 e foi testado com sucesso em diferentes aplicações na indústria de alimentos, conforme reportado em trabalhos científicos.
A água eletrolisada (EW), um sanitizante produzido a partir da água com cloreto de sódio (NaCl) sem adição de produtos químicos nocivos, tem mostrado grande potencial como substituto do hipoclorito de sódio (NaClO), produzindo danos mais severos nas células bacterianas em comparação com a desinfecção com cloro puro. A aplicação de EW em ambientes de processamento de alimentos tem várias vantagens, incluindo custo-benefício, produção in loco, além de ser seguro para a saúde humana.
Quando, a este processo de obtenção de água eletrolisada, é inserida uma membrana de separação (também chamada de diafragma), pode-se produzir dois tipos de solução, sendo uma de pH ácido (anólito) e outra alcalina (católito). Íons com cargas positivas (H+ e Na+) são atraídos pelo cátodo, tornando-se, ao receber elétrons, gás hidrogênio (H2) e hidróxido de sódio (NaOH).
Já os íons com carga negativa (OH– e Cl–) são atraídos pelo ânodo doando elétrons e resultando em cloro gasoso (Cl2), gás oxigênio (O2), íon hipoclorito (OCl–) e ácido hipocloroso (HClO). A figura 1 representa este processo:
Figura 1: Processo de eletrólise de solução salina
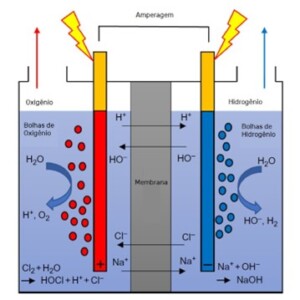
Fonte: Shiroodi e Ovissipour, 2018
No lado do ânodo, forma-se uma solução ácida (chamada anólito) com pH entre 2 e 3 e potencial de oxirredução maior que 1000 mV e entre 10 e 90 ppm de cloro ativo, dependendo da concentração de sal na solução inicial.
No lado do cátodo, forma-se uma solução alcalina (também chamada católito) com pH na faixa de 10 a 13 e potencial de oxirredução entre 800 e 900 mV.
Variações desse sistema, com adição de ácido clorídrico ou íons hidróxido, permitem a obtenção de soluções em outras faixas de pH.
Recentemente, indústrias e pesquisadores relataram a geração de água eletrolisada neutra (NEW) com um pH de 7-8, e ORP de 750–1000mV e água eletrolisada levemente ácida (SAEW) com pH de 5 a 6,5 e ORP de aproximadamente 850mV.
A NEW é produzida pela mistura da solução anódica com íons OH_ ou por eletrólise de NaCl em uma unidade de célula única, enquanto SAEW é gerada pela eletrólise de HCl sozinho ou em combinação com NaCl em uma unidade de célula única.
Em termos gerais, as nomenclaturas mais utilizadas nos artigos são:

Tabela 1 – Siglas e abreviações mais utilizadas nos artigos técnicos relacionados a água eletrolisada
Apesar dos resultados em relação à ação bactericida da AEW serem favoráveis, o processo AEW pode gerar gases (Cl2) que são tóxicos aos manipuladores, restringindo o uso em nível industrial.
A atividade antimicrobiana da água eletrolisada depende muito do pH e de como o pH pode determinar a forma disponível de cloro. O ácido hipocloroso (HClO) é a forma mais forte de cloro, que pode chegar a 80 vezes mais que o hipoclorito (ClO–) quando o pH está próximo 5–6,5. Em pH mais baixo, o HClO é dissociado em gás cloro Cl2, e em pH mais alto forma ClO-. (Fig. 2).
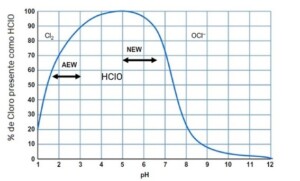
Figura 2. Relação entre pH e formas disponíveis de cloro.
Espécies de cloro ativo, incluindo Cl2, ClO–, e HClO, contribuem para a inativação microbiana. Pesquisadores concluíram que a principal razão para a inativação das bactérias são as propriedades de penetração do HClO e ClO–. ClO ionizado– não é capaz de penetrar na membrana da célula microbiana devido à existência da bicamada lipídica hidrofóbica e algumas estruturas protetoras da parede celular, e o fato de que a célula de uma bactéria patogênica é carregada negativamente por natureza. A carga dos íons negativos de hipoclorito (ClO–) será repelida pela carga negativa da parede celular da bactéria patogênica, resultando em ação oxidante fraca apenas fora da célula.
A forma neutra do ácido hipocloroso HClO pode penetrar na parede celular do microrganismo patogênico com muita facilidade, tornando-se assim um desinfetante muito eficaz que pode atuar tanto no exterior como no interior do microrganismo. O ácido hipocloroso também pode penetrar nas camadas de limo, paredes celulares e camadas protetoras de microrganismos. Além disso, o ácido hipocloroso pode matar as bactérias oxidando grupos sulfidrila de certas enzimas, interrompendo a síntese de proteínas e descarboxilação de aminoácidos a nitritos e aldeídos.
A corrente elétrica, a vazão de água e a concentração de sal também afetam as propriedades da água eletrolisada produzida. O aumento da vazão de água causa um aumento na corrente elétrica devido à eletrólise de mais solução salina. Aumentar a redução bacteriana aumentando a taxa de fluxo de água foi relatado para E. coli e L. monocytogenes. A concentração de sal tem relação linear com a concentração de cloro.
Alguns equipamentos, além de produzir a água eletrolisada levemente ácida SAEW, também produzem o BEW, que devido a sua composição de hidróxido de sódio pode ser estudado futuramente como detergente e aplicado antes da desinfecção para limpeza, por exemplo, de superfícies. Resíduos orgânicos diminuem a eficácia de redução microbiológica pelo ácido hipocloroso.
Em um trabalho de revisão de aplicações de água eletrolisada como agente de limpeza e desinfecção, pesquisadores relataram que essa é uma solução promissora para a indústria de alimentos e bebidas, podendo ser aplicada sozinha ou combinada com outras técnicas de desinfecção como ultrassom, ultravioleta e tratamento térmico.
A água eletrolisada EW é reconhecida por órgãos norte-americanos como FDA (Food and Drug Administration, agência norte-americana reguladora dos setores alimentícios e de medicamentos), USEPA (United States Environmental Protection Agency, Agência de Proteção Ambiental) e (United States Department of Agriculture, Departamento da Agricultura dos Estados Unidos) para fins de descontaminação de superfícies e no processamento de alimentos. Além disso, foi reconhecida como desinfetante para utilização em produtos orgânicos pelo USDA, em 2015.
Vantagens e desvantagens da água eletrolisada
As vantagens da água eletrolisada são muitas em comparação com outras tecnologias de sanitização:
- Pode ser gerada no local e é relativamente barata.
- Fornece água eletrolisada com qualidade consistente, que também pode ser armazenada por até 6 meses.
- Pode ser produzido por eletrólise de água com solução salina diluída, como NaCl, o que o torna seguro para o meio ambiente.
- Sua aplicação reduz os problemas de segurança e custo com manuseio, armazenamento e aplicação de solução de cloro.
- No caso da água eletrolisada levemente ácida SAEW e neutra NEW são mais segura para operadores e funcionários pois não gera gás cloro.
- Atualmente é possível obter água eletrolisada levemente ácida SAEW com 500 ppm e é fácil modificar a concentração de cloro para atingir as concentrações desejadas com base na aplicação.
- Pode ser convertido para a água normal após a aplicação, sem liberar gases prejudiciais.
- Segundo alguns pesquisadores, a água eletrolisada não causa resistência em microrganismos
- É mais eficaz que o cloro. Consequentemente, a formação de cloraminas e trialometanos é menor.
- Também pode evitar o escurecimento enzimático durante o armazenamento de alimentos em atmosfera modificada embalagem.
- A água eletrolisada tem menos citotoxicidade e menos impacto nos atributos de qualidade de materiais alimentares. No caso da SAEW, é menos corrosiva e tem menor impacto na qualidade em comparação com outras soluções ácidas.
- NEW tem muitas vantagens devido ao seu pH neutro e à forma de cloro disponível.
- A NEW obteve o certificado do Departamento de Agricultura dos EUA (DA) como Produto orgânico.
A água eletrolisada, semelhante a outras tecnologias, tem suas próprias desvantagens:
- AEW, pH <3, pode ser corrosivo para alguns metais e resinas sintéticas.
- Sua eficácia diminui significativamente quando entra em contato com materiais orgânicos particularmente proteínas devido à sua reação com proteína.
- No caso de AEW, pH <3, a máquina pode gerar gás cloro que não é seguro para o operador.
- O equipamento pode ser um investimento inicial alto.
Aplicações em indústria de alimentos
Algumas aplicações possíveis do ácido hipocloroso nas indústrias:
- Desinfecção de superfícies
- Limpeza de circuitos fechados – CIP
- Lavagem de caixas plásticas de transporte
- Lavagem e desinfecção de frutas e ovos
- Lava-botas ou barreiras de contenção (superfícies dos calçados)
- Nebulização e sanitização por “neblina” de áreas/cantos de difícil acesso.
E no Brasil?
Segundo levantamento de estudos e artigos publicados em vários países, a utilização dessa tecnologia no Brasil é menor do que 1%, conforme apresentado na Figura 3.
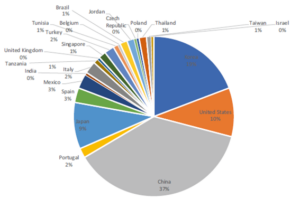
Figura 3: Artigos publicados sobre a utilização de água eletrolisada
Fonte: Iram at all, 2021
Para atender a legislação brasileira para Saneantes (RDC 14/2007), que está em conformidade com a AOAC – referente a Desinfetantes para indústria de Alimentos, foram realizados testes de eficácia de redução microbiológica e para aprovação devem apresentar uma redução mínima de 5 log. Os testes foram realizados em laboratório acreditado no Brasil com água eletrolisada levemente ácida SAEW, pH 5,35 / 5,68 e 500 ppm de ácido hipocloroso e tempo de contato de 10 minutos. Foram aprovados e estão demonstrados na Tabela 2.

Tabela 2: Resultados fornecidos por laboratório acreditado
Assim, podemos concluir que as indústrias brasileiras têm muito a desenvolver com a nova tecnologia sustentável que o ácido hipocloroso oferece, com várias vantagens ambientais e visando maior segurança dos alimentos.
Leia também:
· Referências
Ruviaro, A. R. 2017. O papel da água eletrolisada na segurança dos alimentos.
Al Haq, M.I., Sugiyama, J., Isobe, S., 2005. Applications of electrolyzed water in agriculture & food industries. Food Sci. Technol. Res. 11 (2), 135–150.
· Audenaert, K., Monbaliu, S., Deschuyffeleer, N., Maene, P., Vekeman, F., Haesaert, G., De Saeger, S., Eeckhout, M., 2012. Neutralized electrolyzed water efficiency reduces Fusarium spp. in vitro and on
· Ayebah, B., Hung, Y.C., Frank, J.F., 2005. Enhancing the bactericidal effect of electrolyzed water on Listeria monocytogenes biofilms formed on stainless steel. J. Food Protect. 68, 1375–1380.
· Bird MR, Fryer PJ (1991) An experimental study of the cleaning of surfaces fouled by whey proteins. Food Bioprod Process 69:13–21
· Deza, M., Araujo, M., Garrido, M., 2003. Inactivation of Escherichia coli O157:H7, Salmonella enteritidis and Listeria monocytogenes on the surface of tomatoes by neutral electrolyzed water. Lett. Appl. Microbiol. 37 (6), 482–487
· Deza, M.A., Araujo, M., Garrido, M.J., 2005. Inactivation of Escherichia coli, Listeria monocytogenes, Pseudomonas aeruginosa and Staphylococcus aureus on stainless steel and glass surfaces by neutral electrolysed water. Lett. Appl. Microbiol. 40, 341–346. https://doi.org/10.1111/j.1472-765X.2005.01679.x.
· Forghani, F., Park, J.-H., Oh, D.-H., 2015. Effect of water hardness on the production and microbicidal efficacy of slightly acidic electrolyzed water. Food Microbiol. 48, 28–34.
· Fukuzaki, S., 2006. Mechanisms of actions of sodium hypochlorite in cleaning and disinfection processes. Biocontrol Sci. 11 (4), 147–157.
· Gomez-Lopez, V.M., Ragaert, P., Ryckeboer, J., Jeyachchandran, V., Debevere, J., Devlieghere, F., 2007. Shelf-life of minimally processed cabbage treated with neutral electrolyzed oxidizing water and stored under equilibrium modified atmosphere. Int. J. Food Microbiol. 117 (1), 91–98.
· Hao X.X., B. M. Li , C. Y. Wang , Q. Zhang and W. Cao. 2013. Application of slightly acidic electrolyzed water for inactivating microbes in a layer breeding house. Poultry Science 92 :2560–2566
· Hinton, A.Jr., Northcutt, J. K., Smith, D. P., Musgrove, M. T., and Ingram, K. D. 2007. Spoilage Microflora of Broiler Carcasses Washed with Electrolyzed Oxidizing or Chlorinated Water Using an Inside-Outside Bird Washer
· Hricova D., R. Stephan, and C. Zweifel. 2008. Eletrolyzed water and its application in the food industry. J of Food Protection. Vol. 71. No 9 Pages 1934-1947.
· Hsu, S.-Y., 2003. Effects of water flow rate, salt concentration and water temperature on efficiency of na electrolyzed oxidizing water generator. J. Food Eng. 60 (4), 469–473.
· Iram, A., Wang, X., Demirci, A., 2021. Electrolyzed Oxidizing Water and Its Applications as Sanitation and Cleaning Agent. Food Engineering Reviews 13:411–427
· Issa-Zacharia, A., Kamitani, Y., Miwa, N., Muhimbula, H., Iwasaki, K., 2011. Application of slightly acidic electrolyzed water as a potential nonthermal food sanitizer for decontamination of fresh ready-to-eat vegetables and sprouts. Food Control 22 (3), 601–607.
· Iwasawa, A., Nakamura, Y., 1993. Antimicrobial activity of aqua oxidizing water. Clin. Bacteriol. 20, 469–473.
· Kim, C., Hung, Y.C., Brackett, R.E., Frank, J.F., 2001. Inactivation of Listeria monocytogenes biofilms by electrolyzed oxidizing water. J. Food Process. Preserv. 25, 91–100. https://doi.org/10.1111/j.1745-4549.2001.tb00446.x.
· Koseki, S., Fujiwara, K., Itoh, K., 2002. Decontaminative effect of frozen acidic electrolyzed water on lettuce. J. Food Prot. 65 (2), 411–414.
· Koseki, S., Yoshida, K., Isobe, S., Itoh, K., 2001. Decontamination of lettuce using acidic electrolyzed water. J. Food Prot. 64 (12), 652–658.
· Nan, S., Yongyu, L., Baoming, L., Wang, C., Cui, X., Cao, W., 2010. Effect of slightly acidic electrolyzed water for inactivating Escherichia coli O157:H7 and Staphylococcus aureus analyzed by transmission eléctron microscopy. J. Food Prot. 73 (12), 2211–2216.
· Ovissipour, M., Al-Qadiri, H.M., Sablani, S.S., Govindan, B.N., Al-Alami, N., Rasco, B., 2015. Efficacy of acidic and alkaline electrolyzed water for inactivating Escherichia coli O104:H4, Listeria monocytogenes, Campylobacter jejuni, Aeromonas hydrophila, and Vibrio parahaemolyticus in cell suspensions. Food Control 53, 117–123.
· Possas A., F. P´erez-Rodríguez , F. Tarlak , R. M. García-Gimeno , 2021. Quantifying and modelling the inactivation of Listeria monocytogenes by electrolyzed water on food contact surfaces. J. of Food Engineering. 290: 110287
· Rahman, S.M.E., Khan, I., Oh, D.-H., 2016. Electrolyzed water as a novel sanitizer in the food industry: current trends and future perspective. Compr. Rev. Food Sci. Food Saf. 15, 471–490. https://doi.org/10.1111/1541-4337.12200
· Rahman, S.M.E., Park, J.H., Wang, J., Oh, D.-H., 2012. Stability of low concentration electrolyzed water and its sanitization potential against foodborne pathogens. J. Food Eng. 113 (4), 548–553.
· Ruviaro, A. R. 2017. O papel da água eletrolisada na segurança dos alimentos. https://foodsafetybrazil.org/agua-eletrolisada-na-seguranca-dos-alimentos/
· Santos,R. A,, Garcia R. G., Gandra E. R. S., Burbarelli M. F. C., Muchon, J. L., Caldara, F. R. 2019. Carcass Washing as an Alternative to Trimming – Is It Possible to Use Carcass Washing as an Alternative to Trimming in Commercial Broiler Slaughterhouses in Brazil? Brazilian Journal of Poultry Science. V.22 n.2 001-006 http://dx.doi.org/10.1590/1806-9061-2019-1209
· Shiroodi S. G., Ovissipour M., 2018. Eletrolyzed water application in fresh produce sanitation. Elsevier. Chapter 3, 67-87.
· Wang X, Demirci A, Puri VM, Graves RE (2016) Evaluation of blended electrolyzed oxidizing water-based cleaning-in-place (CIP) technique using a laboratory-scale milking system. Trans ASABE 59:359–370
· Zang, Y. T. , Li, B. M., Bing, Sh. and Cao W. , 2015. Modeling disinfection of plastic poultry transport cages inoculated with Salmonella enteritids by slightly acidic electrolyzed water using response surface methodology Poultry Science 94:2059–2065
· Zhang, J., Wang, J., Zhao, D., Hao, J. 2021. Efficacy of the two-step disinfection with slightly acidic electrolyzed water for reduction of Listeria monocytogenes contamination on food raw materials. LWT 140 (2021) 110699
· FDA & EPA. Certifications of Electrolyzed Water. 2p. 2016 Disponível em: http://www.environize.ca/wp-content/uploads/2015/03/FDA-EPA-Approvals-s.pdf. Acesso em maio de 2017.
· USDA. U.S. Department of Agriculture. National Organic Program. Policy Memorandum. PM 15-4 Electrolyzed Water. In: National Organic Program Handbook: Guidance and Instructions for Accredited Certifying Agents and Certified Operations. 2 p. 2015. Washington, DC. Sept, 11, 2015. Disponível em: https://www.ams.usda.gov/sites/default/files/NOP-PM-15-4-ElectrolyzedWater.pdf. Acesso em maio de 2017.
· https://avinews.com/electrolisis-salina-vs-hipoclorito-sodico/ Revista AviNews Espanha Dezembro 2021
10 min leituraO ácido hipocloroso é um novo e promissor ativo desinfetante com apelo sustentável, porque é obtido pela eletrólise de água e sal e não tem efeitos nocivos ao meio ambiente. […]





