Estamos passando por um momento de crescente atenção da indústria e dos órgãos reguladores em torno de contaminantes formados durante processamentos térmicos de alimentos – entre eles, o 3-MCPD e seus ésteres. Exemplos disso são o código de práticas do Codex Alimentarius, o regulamento da União Europeia e o monitoramento conduzido pela FDA, além da recente inclusão deste contaminante na lista de monitoramento pela Anvisa.
Normalmente o 3-MCPD está associado a óleos vegetais, porém também se mostra potencialmente perigoso nas fórmulas infantis. Diante disso, como a indústria pode controlar esse contaminante de maneira eficaz?
O que é e qual o seu risco?
O 3-MCPDE (3-monocloropropano-1,2-diol éster) é uma molécula de éster que pode ocorrer em óleos vegetais após uma de suas etapas de produção. Durante o refino, o óleo é submetido a um processo térmico que tem como objetivo diminuir ou remover compostos que conferem sabor, odor e cor não esperados no produto terminado.
Esta molécula se transforma em 3-MCPD livre após hidrólise ácida no nosso trato digestivo. Segundo estudos realizados com roedores, o 3-MCPD causa efeitos adversos nos rins e órgãos reprodutores. Em 2013, a International Agency for Research on Cancer (IARC) classificou o 3-MCPD no grupo 2B, o que indica que é possivelmente carcinogênico para humanos.
O tema assume maiores proporções a partir do momento em que se sabe que óleos vegetais são ingredientes de proporções relevantes em fórmulas infantis. Isso levanta o alerta para a necessidade de aplicação de controles deste contaminante na indústria de alimentos, devido à vulnerabilidade deste público consumidor.
- Como mencionado pela colega Cíntia Malagutti, a Joint Expert Committee on Food Additives (JECFA) apresentou os resultados do estudo com as consequências da ingestão de 3-MCPDE e outros compostos, reforçando a necessidade de seu controle.
Com base nisso, a comissão do Codex Alimentarius preparou uma série de recomendações importantes para a indústria de óleos refinados e alimentos, por meio de um código de práticas. Este material inclui dicas que vão desde a agricultura, passando pelo refino, pós refino e medidas de processamento e que podem ser aplicadas de modo a reduzir os níveis de 3-MCPDE e éster glicidílico (GE) em alimentos.
Recomendações e estratégias de mitigação
Antes de passarmos essas orientações é importante saber:
De acordo com este código, as plantas absorvem durante seu desenvolvimento compostos clorados do solo, da água, de fertilizantes e outros. Esses compostos são precursores do 3-MCPDE.
A formação de GE inicia-se em torno de 200°C, com maior taxa a partir de 230°C. Enquanto que a formação de 3-MCPDE ocorre na faixa de 160 – 200°C, não aumentando com o aumento da temperatura.
Devido a seus diferentes mecanismos de formação, as estratégias de mitigação tendem a ser diferentes. No caso do GE, que é formado com temperaturas mais altas, a estratégia é o controle da alta temperatura. Apesar disso, diminuir a temperatura pode alcançar a faixa de formação do 3-MCPDE.
As recomendações indicam combinar medidas para garantir maior efetividade das ações. Essa combinação pode incluir estratégias como a minimização do uso de fertilizantes, pesticidas e água que apresentam excesso de compostos com cloro.
Especificamente no caso de óleo de frutos como a palma, recomenda-se realizar a colheita no momento mais adequado, ou seja, quando apresentam menor concentração da enzima lipase, associada ao processo de formação de 3-MCPDE.
Na indústria, as recomendações envolvem o armazenamento de grãos em temperaturas inferiores a 25°C, com umidade menor que 7%, na busca dos menores índices da enzima lipase. Além disso, recomenda-se monitorar precursores como DAGs (diacilglicerois), FFAs (ácidos graxos livres) e compostos clorados nas etapas de produção do óleo bruto.
Já na etapa de branqueamento, indica-se utilizar maiores quantidades de terra branqueadora, além de evitar aquelas terras que apresentam quantidades significativas de compostos com cloro.
Na desodorização, o ideal para óleos vegetais é manter a faixa de 190 a 230°C. Além disso, recomenda-se aplicar vácuo mais forte para facilitar a remoção dos compostos voláteis, de modo a não ser necessário o aumento da temperatura, o que favoreceria a formação de GE.
- Todas essas medidas e outras estão disponíveis no material do Codex Alimentarius de 2019 (código de referência CXC 79-2019).
No caso de indústrias alimentícias, como as de fórmulas infantis, é importante utilizar óleo com as menores concentrações de 3-MCPDE e GE, de modo a evitar a concentração deste contaminante em seu produto terminado. Isso se dá com o devido processo de homologação de fornecedores, bem como medidas de controle para o recebimento de matérias-primas.
O monitoramento e regulamentações
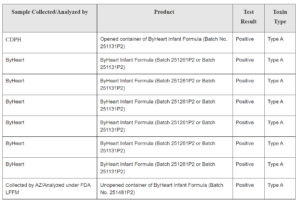
O FDA estabeleceu métodos laboratoriais de monitoramento de 3-MCPDE e GE, inicialmente com foco nas fórmulas infantis. Entre os anos de 2013 e 2016 foram avaliadas 98 amostras de fórmulas. A partir de então, o órgão iniciou conversas com o segmento industrial para apresentar suas preocupações.
Na sequência, entre 2017 e 2019, com o objetivo de avaliar se os fabricantes reduziram o nível de 3-MCPDE e GE nas fórmulas infantis, novas 222 amostras foram avaliadas, sendo que 3 fabricantes apresentaram sucesso na redução.
Já entre 2021 e 2023, outras 206 amostras foram analisadas, o que indicou que todos os 4 fabricantes avaliados reduziram o nível dos referidos contaminantes a níveis consistentes internacionalmente.
Apesar dos limites não serem definidos na legislação estadunidense, a União Europeia define tais limites claramente para óleo, gorduras e alimentos para lactentes através do Regulamento (EU) 2023/915.
Já no Brasil, a ANVISA publicou em março de 2025 a IN 351 que complementa a IN 160 de 2022. Ela estabelece limites máximos tolerados de contaminantes em alimentos, incluindo o 3-MCPD. Porém, por enquanto este contaminante está indicado apenas para condimentos líquidos contendo proteínas vegetais hidrolisadas ácidas, com prazo de implementação findando em março de 2026.
Notícias recentes indicam a ocorrência e a relevância desses controles não apenas nos óleos, gorduras e alimentos infantis. Em julho de 2025, a Coreia procedeu um recall de molhos de soja devido ao alto índice de 3-MCPD em sua composição.
Importante reforçar que o 3-MCPD e seus ésteres não são inevitáveis, uma vez que o controle é possível aplicando uma gestão adequada e focada. Além disso, um trabalho preventivo e sistêmico iniciando na agricultura tende a minimizar os impactos na indústria.
Essas estratégias vão ao encontro da tendência percebida globalmente no monitoramento deste contaminante. Assim, a indústria que alia a ciência, a tecnologia e um sistema de gestão direcionado garante não apenas conformidade com a legislação, como também abertura em um mercado cada dia mais exigente e informado.
Imagem: Kaboompics
4 min leituraEstamos passando por um momento de crescente atenção da indústria e dos órgãos reguladores em torno de contaminantes formados durante processamentos térmicos de alimentos – entre eles, o 3-MCPD e […]